定義
在給定環境(T,P)下,能量可轉變為有用功的部分稱為有效能,餘下的不能轉變為有用功的部分稱為無效能。
計算
對於恆溫熱量Q,其有效能部分為
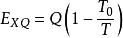 無效能
無效能無效能部分則為
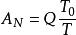 無效能
無效能當熱量Q的溫度降至環境溫度T時,則全部熱量都變成無效能,即E=0,A=Q。因此,環境溫度T下的熱量是不能轉化為功的。
處於某狀態的焓H,可以根據穩定流動過程的物系有效能計算式求取
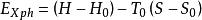 無效能
無效能則其無效能為
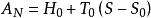 無效能
無效能與有效能
系統的總能量E由有效能(E)與無效能(A)兩部分組成,即
E=E+A
dE=d(E+A)
根據熱力學第一定律,系統的總能量是守恆的,因此
dE=d(E+A)=0。
根據熱力學第二定律,對於不可逆過程,有效能要減少;只有可逆過程,有效能才是守恆的。不可逆過程總能量守恆而有效能減少,那么無效能必定要增加。有效能減少的量就是無效能增加的量,即
dE=-dA
