病毒歷史
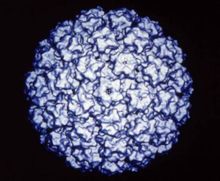 人類乳頭瘤病毒
人類乳頭瘤病毒 人類乳頭狀瘤病毒(Humanpapillomavirus,HPV)是一種嗜上皮性病毒,在人和動物中分布廣泛,有高度的特異性,長期以來,已知HPV可引起人類良性的腫瘤和疣,如生長在生殖器官附近皮膚和黏膜上的人類尋常疣、尖銳濕疣以及生長在黏膜上的乳頭狀瘤。自從1976年zurHansen提出HPV可能是性傳播致癌因素以來,HPV感染與宮頸癌關係的研究成為腫瘤病毒病因研究的熱門課題。
公元610年(隋代),我國著名醫家巢元方撰寫的《諸病源候論 癭瘤等病諸候 疣目候》中記載:“疣目者,人手足邊或生如豆,或如結筋,或五個或十個相連肌里,粗強於肉,謂之疣目。”對疣目(尋常疣)的好發部位和皮損形態進行了描述。
1907年發現乳頭瘤病毒是皮膚疣的病原。
1933年Shope在綿尾兔體內首次發現乳頭瘤病毒(cottontial rabbit papillomavirus,CRPV),隨後相繼在人和各種動物中發現了乳頭瘤病毒。
預防疫苗摺疊
全球首支HPV疫苗已2006年在美國上市,7年間,100多個國家套用HPV疫苗,大幅降低HPV患病率和癌前病變發生率,HPV疫苗在中國的上市審批也已進入三期臨床試驗階段,已上市兩種HPV疫苗,一種是四價疫苗,針對HPV-6、HPV-11、HPV-16和HPV-18這4型病毒;另一種是二價疫苗,只針對HPV-16和HPV-18,其中HPV-16和HPV-18都是會引起宮頸癌的高危型HPV。
疫苗並未在中國內地上市,接種疫苗需通過美亞預約網預約赴港進行。
hpv疫苗能預防包括hpv6,11,16,18在內的四種亞型,同時防止由這四種病毒引起的子宮頸癌、陰道癌、外陰癌以及生殖器官濕疣等相關疾病。
預防HPV感染最好的辦法是不與任何的生殖器接觸,但這是很難辦到的,即使戴了保險套,未被保險套復蓋的區域也可能造成感染。據悉,女生如果大學一年換一個男朋友,畢業時被HPV感染的機率超過85%。 一個簡單可行的辦法是,與自己的性伴侶保持長期、固定的關係是最大限度地預防生殖器HPV感染的有效措施。然而,即便如此還是很難明確性伴侶以前是否感染過。
病原特徵
1.HPV為乳多空病毒科A屬成員,是一類感染表皮和黏膜鱗狀上皮的小DNA病毒。
2.直徑52-55nm,無被膜,正20面體結構,表面有72個殼體。病毒基因組是雙鏈環狀DNA分子。
3.具有高度種屬特異性,人類皮膚角質形成細胞/黏膜鱗狀上皮細胞的是其天然宿主。
4.具有特殊嗜上皮性,僅在一定分化程度的上皮細胞內增殖。
5.不經血流擴散,不產生病毒血症,也不易被免疫系統識別。
6.根據HPV的同源性,已發現120多種型別。
相關腫瘤
光線性角化病,皮膚鱗癌,基底細胞癌,惡性黑素瘤,脂溢性角化病,毛鞘囊腫,生乳頭汗管囊腺瘤,多發性跖部表皮囊腫,硬化性苔蘚,砷角化病,汗管瘤,眼部腫瘤(眼乳頭狀瘤、鱗狀細胞癌、視網膜母細胞瘤),宮頸癌, 食管癌,肺癌。
疣角關係
1.皮角是一個臨床病名,多在其它皮膚病基礎上發生。
2.引起皮角的基礎疾病有:尋常疣、脂溢性角化病、汗孔角化病、疣狀痣、角化棘皮瘤、外毛根鞘瘤、倒置性毛囊角化病、基底細胞上皮瘤、皮脂腺腺瘤、良性血管瘤、日光角化病、早期皮膚鱗癌等。皮角的基礎疾病中尋常疣占15-23%;約50%的皮角發生於良性損害之上,23-37%發生於光線性角化(癌前病變)損害之上,16-20%發生於惡性損害之上。
3.與惡性病變或癌前病變相關聯的皮角具有以下4種特徵:
①皮角基底呈惡性病變或癌前病變者平均年齡比良性病變者大8.9歲;
②男性更易發生;
③惡性或癌前病變的70%以上發生於鼻部、耳廓、手背、頭皮、前臂和面部;
④幾何形態呈寬基底、低高度的皮角損害。
免疫關係
一般認為疣的病程與機體免疫特別是細胞免疫功能低下密切相關,患有腎移植、惡性淋巴瘤、愛滋病等有免疫缺陷的患者疣發病率增高、病損數目多、病程延長。
免疫逃逸機制 /“擊中-逃逸”機制
機體雖然有一整套完善的免疫系統防禦各種微生物包括病毒感染。但是HPV在與人類共同進化的漫長過程中,形成了從天然免疫(炎症反應,細胞因子如干擾素、白介素-18等)到獲得性免疫(病毒抗原的捕獲及呈遞,特異性T細胞免疫應答)的多層次免疫逃逸機制。因此臨床上可以看到部分細胞免疫功能正常者發生HPV感染性疾病。
從天然免疫的逃逸機制:
①HPV感染有增殖能力的基底細胞,並嚴格隨角質形成細胞的角化過程、分化成熟而開始進行病毒早期和晚期基因的轉錄翻譯,組裝形成病毒顆粒,並隨皮屑排泄而脫落。這些角質形成細胞是注定要死亡的,故不引起顯著的炎症反應,免疫系統會忽視或漠視這種病毒感染。
②HPV能使IFN、IL-18的表達及作用下調,導致相應的NK細胞和局部組織的巨噬細胞的吞噬功能下降。
從獲得性免疫的逃逸機制:
① 在HPV感染上皮中,朗格漢斯細胞(LC)數量減少、結構發生改變,造成HPV抗原提呈障礙。
② LC多位於表皮基底層,而人類乳頭瘤病毒的早期基因產物多見於成熟的角質形成細胞即位於表皮中上層中, 位於胞核中,而且呈低水平表達;晚期基因產物在終末細胞的胞漿和胞核內表達,但這些細胞很快會脫落,使得LC接觸病毒抗原的機會減小。
③HPV衣殼抗原,尤其是E7可以降低特異性CD4+T細胞對朗格漢斯細胞反應。
④ HPVE7蛋白在皮膚角質形成細胞的表達可誘導E7特異性的細胞毒性T淋巴細胞(CTL)前體細胞耐受,因此不能發揮有效的細胞毒作用。
發病機制
HPV感染與致癌機制與感染的HPV型別、病毒致癌產物、病毒基因與宿主細胞的整合、機體的免疫狀態、病毒的免疫逃逸以及紫外線照射等因素密切相關,往往是多種因素相互作用的結果。
早期HPV通過皮膚黏膜微小損傷侵入有增殖能力的基底細胞。
具有增殖能力的基底幹細胞的感染是導致復發或持續性病變的前提條件。
病毒以染色體外或整合到宿主染色體的方式存在。
病毒E6、E7蛋白抑制正常凋亡過程,誘導細胞分裂周期加快,出現乳頭瘤改變。
病毒主要集中在顆粒層中的細胞核內,在表皮的顆粒層出現挖空細胞。病毒隨表皮更新而排除體外,可造成自身接種傳染或人與人之間的傳染。
病毒通過釋放某些蛋白影響皮膚局部抗原呈遞,導致病毒的免疫逃逸。
高危型HPVE6、E7蛋白能與p53等抑癌物質結合併促其降解,而誘發皮膚癌。
病毒DNA整合進入宿主染色體,導致宿主染色體不穩定、DNA複製轉錄紊亂而引發腫瘤。
暴光部位的皮膚損害,由於紫外線長期照射可使癌變過程加速。
從被感染到發生疣狀/乳頭瘤狀損害的潛伏期為數周到數年,平均約3個月。無症狀亞臨床感染亦多見。疣的自愈率為:2個月23%、3個月30%、2年65-78%。
病理改變
1.角化過度伴角化不全,棘層肥厚,呈外生性乳頭瘤樣增生。
2.棘層上部和顆粒層內見灶狀空泡化細胞(挖空細胞)。
3.基底膜完整。
4.HPV免疫組化檢測:棘層上部、顆粒層細胞核和角質層角化不全細胞核陽性。
5.真皮單一核細胞浸潤,疣消退時明顯。
挖空細胞形態:
1)尋常疣:挖空細胞灶狀分布,核較小、深染。表皮上部細胞質內有明顯角質透明顆粒聚集。
2)扁平疣:挖空細胞瀰漫性分布,大小一致。
3)疣狀表皮發育不良: 挖空細胞瀰漫或灶狀分布,細胞質空泡化或泡沫化,細胞核固縮、核染色質邊緣分布、核內空泡,細胞大小不一,呈“發育不良”外觀。表皮基底部可見角化不良細胞。
4)尖銳濕疣:挖空細胞胞體和胞核均較大,核深染,呈貓眼狀。
5)深部掌跖疣:挖空細胞灶狀分布,表皮細胞的胞質中含有大量嗜酸性透明角質顆粒。
病毒結構
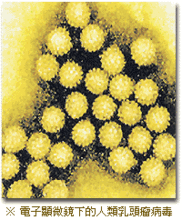 電子顯微鏡下的人類乳頭瘤病毒
電子顯微鏡下的人類乳頭瘤病毒 人類乳頭瘤病毒(HPV)。屬DNA病毒。人體皮膚及黏膜的復層鱗狀上皮上HPV的唯—宿
主,尚未在體外培養成功。病毒顆粒直徑為45~55nm。這是非常小的,一般光學顯微鏡是不能看到的,只有藉助電子顯微鏡才能看到。人類乳頭瘤病毒的類型很多,分子生物學技術研究發展迅速,證實人類乳頭瘤病毒有60種以上的抗原型,即這一家族裡有60多個相似而又不同的病毒(亞型),其中至少有10個類型與尖銳濕疣有關(如6,11,16,18及33型,最常見6、11型),而第11,16,18型,則是國外目前研究宮頸癌、外陰癌甚至陰莖癌的最熱門的病毒因子,其長期感染與女性宮頸癌的發生有關。尖銳濕疣與尋常疣、扁平疣、絲狀疣、掌跖疣等,同為感染人類乳頭瘤病毒(HPV)引起。但不同類型的HPV能引起不同的疣。如Ⅰ型主要引起掌跖疣,Ⅱ型主要引起尋常疣,Ⅲ型主要引起扁平疣,而尖銳濕疣主要是由Ⅵ型、Ⅺ型病毒感染所引起。HPV在溫暖潮濕的環境中特別易生存增殖,故男女兩性的外生殖器是最易感染的部位。病毒可自身接種,因此發生於肛門等部位的損害常出現於兩側接觸面。
HPV為乳多空病毒科A屬成員,病毒顆粒直徑45-55nm無被膜的正20面體構成的病毒殼體,具有7900鹼基對的環狀雙鏈DNA組成,電鏡下病毒顆粒的大小、形態與口多瘤病毒極為相似。乳頭瘤病毒(PV)具有種屬特異性,HPV尚未能在組織培養或實驗動物模型中繁殖。
病毒的結構蛋白組成:85%的PV顆粒,經十二烷基硫酸鈉聚丙烯醯胺凝膠電泳(SDS——PAGE)可確定病毒有主要衣殼蛋白、分子量為56.000;次要衣殼蛋白,分子量遷移於76.000處,發現4種細胞組蛋白與病毒DNA相關。
所有HPV病毒的基因組結構相似,根據在嚴格條件下進行DNA雜交的程式可確定病毒的型和亞型,不同的HPV型DNA與其他類型病毒DNA僅50%出現交叉雜交,迄今已發現60多種HPV類型,隨著研究的深入,將會鑑定出更多HPV新的類型。
生物性狀
HPV是一種小的DNA病毒,直徑45~55nm,衣殼呈二十面體立體對稱,含72個殼微粒,沒有囊膜,完整的病毒顆粒在氯化銫中浮密度為1.34g/ml,在密度梯度離心時易與無DNA的空殼(密度1.29g/ml)分開。
HPV基因組是一閉環雙股DNA,分子量5×106道爾頓。按功能可分為早期區(E區)、晚期區(L區)和非編碼區(NCR)三個區域。E區分為E1~E7開放閱讀框架,主要編碼與病毒複製、轉錄、調控和細胞轉化有關的蛋白。L區分L1和L2,分別編碼主要衣殼蛋白和次要衣殼蛋白。NCR是E區與L區間-6.4~1.0bp的DNA片段,可負責轉錄和複製的調控。
通過對HPV克隆基因的DNA雜交試驗及酶譜分析,以核苷酸同源性少於50%定為新型別,至今已鑑定出70多型HPV。每一型別都與體內特定感染部位和病變有關。HPV各型之間有共同抗原,即屬特異性抗原,存在於L1蛋白, 它與牛乳頭病毒(BPV)有交叉反應。L2蛋白為型特異性抗原,各型間不發生交叉反應。
HPV在體外細胞培養尚未完成。它具有宿主和組織特異性,只能感染人的皮膚和黏膜,不能感染動物。HPV感染後在細胞核內增殖,細胞核著色深,核周圍有一不著色的空暈,此種病變細胞稱為空泡細胞(Koilocytoticcell)。
致病免疫
致病性
 人類乳頭瘤病毒DNA
人類乳頭瘤病毒DNA HPV主要通過直接或間接接觸污染物品或性傳播感染人類。
病毒侵入人體後,停留於感染部位的皮膚和黏膜中,不產生病毒血症。臨床常見的有:尋常疣(主要為1,2,4型)稱刺瘊,可發生於任何部位,以手部最常見。跖疣(主要為2,4型)生長在胼胝下面,行走易引起疼痛。扁平疣(主要為3,10型)好發於面部,手、臂、膝、為多發性。尖性濕疣(主要為6,11型),好發於溫暖潮濕部位,以生殖器濕疣發病率最高,傳染性強,在性傳播疾病中有重要地位,且有惡性變的報導。研究資料證明HPV與宮頸癌、喉癌、舌癌等發生有關。如HPV16,18,33等型與宮頸癌的發生關係密切,用核酸雜交方法檢出癌組織中HPVDNA陽性率60%以上。
免疫性
有關HPV免疫反應研究較少。在感染病灶出現1~2月內,血清內出現抗體,陽性率為50-90%,病灶消退後,抗體尚維持續數月到數年,但無保護作用。用白細胞移動抑制和淋巴細胞轉化等試驗檢測細胞免疫(CMI)的結果不一致,有人觀察到病灶消退時CMI增強。
生物診斷
疣的診斷主要依靠臨床特點,對不能確診的病例,可選下列各種方法輔助診斷。
染色鏡檢
將疣狀物作組織切片或生殖道局部粘液塗片,用帕尼科拉染劑染色後,光鏡下觀察到特徵性空泡細胞或角化不良細胞和角化過度細胞,可初步HPV診斷。
檢測HPVDNA
根據不同標本採用點雜交或原位雜交檢測HPV-DNA。亦可選擇適當的特異序列,合成引物做PCR後進行雜交,PCR具有敏感,特異及可選擇不同型別的引物擴增後分型等優點。
血清學試驗
套用重組技術表達抗原檢測患者血清中lgG抗體。或抗原免疫動物製備免疫血清或單克隆抗體檢測組織或局部粘液中HPV抗原。
防治原則
尚無特異預防方法,可根據HPV傳染方式,切斷傳播途徑,是有效的預防措施。小的皮膚疣有自行消退的可能,一般無需處理。尖性濕疣病損範圍大,可施行手術,但常規外科切除有較高復發率。一些物理療法如電烙術、雷射治療、液氮冷凍療法,有較好的治療效果。用干擾素治生殖器HPV感染,結合上述一些輔助療法,認為有廣闊前景。
流行因素
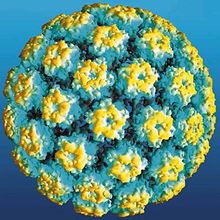 人類乳頭瘤病毒
人類乳頭瘤病毒 由於HPV感染通常沒有明顯的臨床症狀,其檢出率因各種方法而異,對於HPV感染流行因素的分析就很難確定。但HPV感染是一種性傳播疾病,與性行為因素有關,這一點已經明確。而個體的衛生狀況好,注意經期衛生,同房前後衛生,使用宮內避孕環等均可以使感染HPV的幾率降低。
性行為
大部分研究表明婦女的性伴侶數,性交頻率,性伴侶患有生殖道疣等均與HPV感染密切相關。儘管有些研究表明初次性交年齡與HPV感染也有關,但這種因素受性伴侶數的影響,調整性伴侶數後,其危險性無顯著性意義。
免疫因素
宿主的免疫力對HPV感染及病變的進展有很大的作用。有研究發現腎移植的免疫抑制者HPV的感染率是正常人群的17倍。HIV感染的人群中HPV感染率也增高。由於HIV感染人群性行為比較混亂,伴侶數較多,初次性交年齡小等因素,使HPV感染幾率增加。但有些研究並不能證明免疫抑制與HPV感染有直接的相關性,HIV人群可能由於自身暴露的危險性高或機體抵禦潛伏病毒的能力降低而使HPV感染率增高,這一人群的HPVDNA檢出水平高於正常人群,這表明機體抑制HPV感染的能力降低。
懷孕
有研究表明,婦女懷孕次數增多,分娩次數,流產次數等並不增加HPV感染的危險性,畸胎的個數卻與HPV感染相關。有些研究表明孕期婦女HPV感染率高,而且病毒檢出量也增高,但這可能是由於孕期病毒水平增高而使檢出效率提高所致。一項套用PCR法檢測HPV的研究證實了這一觀點,PCR法檢測HPV病毒不依賴病毒的含量,結果發現孕期與非孕期婦女的感染率無顯著差(9.6%/10.9%)。
口服避孕藥
儘管口服避孕藥可以增加宮頸癌的危險性,但它是否影響HPV感染還存在很大爭議。有研究表明口服避孕藥確實能增加HPV感染的幾率,但有人認為口服避孕藥對宮頸低度病變的發生無影響,卻可以增加高度病變的危險性,因此認為口服避孕藥是通過改變疾病的進展狀態,而不是直接影響HPV感染率。
病毒關係
 人類乳頭瘤病毒
人類乳頭瘤病毒 HPV感染與宮頸癌的關係最初在19世紀70年代提出,此後許多流行病學和分子學研究均毫無疑問的證實了HPV與宮頸癌的病因學聯繫。Bosch和Manos等通過收集來自22個國家的宮頸癌活檢標本作PCR檢測,發現99.7%的腫瘤中都可以檢測到HPVDNA,而且各國間無顯著差異。這是迄今為止所報導人類腫瘤致病因素中的最高檢出百分數,同時表明HPV感染與宮頸癌的相關具有普遍意義。
病例-對照研究是檢驗病因假說的一種分析流行病學方法。不論是在拉丁美洲採用準確性較低的檢測技術(FISH)進行的大規模流行病學研究,還是採用較高靈敏度檢測技術(PCR,HC-II)的研究,所有的結果均顯示HPV感染與宮頸癌有明顯的相關性(OR=3.6-254.2),尤其是HPV16型和18型。Muňoz等在哥倫比亞和西班牙(宮頸癌發病率前者比後者高8倍)進行的人群基礎上的病例-對照研究中,包括436例組織學確診的病例和隨機抽取的387例來自病例所在人群的對照,同時採用了三種HPVDNA檢測技術(ViraPap、SH和PCR)。這一研究避免了人群和地區的選擇性偏移,同時又考慮到檢測技術間的差異,在調整了一些混雜因素後三種檢測方法都得出相同的結論:在兩個國家中HPV16,18,31,33和35型與宮頸癌均呈強相關性,提示HPV與宮頸癌具有病因關係。佇列研究是用來驗證疾病病因假說另一種重要的分析流行病學方法,它能夠直接體現HPV感染與宮頸癌發生的時序性,更有力地驗證病因假說。Campion對100例輕度宮頸上皮內病變(CINI)隨訪了兩年多,56%的HPV16,18陽性者進展為重度宮頸上皮內病變(CINIII),而HPV6陽性的對象僅20%發生進展。Murthy等用原位雜交方法的研究顯示,63例宮頸不典型增生髮展為原位癌,對組織標本檢測HPV16/18,陽性率為68.3%,而44例非進展性不典型增生其陽性率為27.3%,相對危險度為5.9(95%CI:2.5-14.1),具有顯著的統計學意義。此外,在細胞學和分子生物學方面也獲得了人乳頭狀瘤病毒致癌的有力證據。1995年WHO和IARC已將HPV確定為是宮頸癌的病因。
生殖道感染HPV最常見的型別即16,18,6,11型。HPV6和11型經常感染外陰、肛門、陰道等部位,屬於低危型別,濕疣或宮頸上皮內低度病變婦女中多常見,與宮頸浸潤癌無明顯關聯;而16和18型則屬於高危型別。來自世界各國的宮頸癌組織標本的研究發現,HPV16和18型感染率最高,在檢出的所有型別中,HPV16占50%,HPV18占14%,HPV45占8%,HPV31占5%,其它型別的HPV占23%。HPV的型別與宮頸癌的病理類型有關,在宮頸鱗狀上皮細胞癌中HPV16占主要地位(51%的鱗狀上皮細胞癌標本),而在宮頸腺狀上皮細胞癌(56%腺狀上皮細胞癌標本)和宮頸腺鱗細胞癌(39%腺鱗細胞癌標本)中HPV18占主要地位。HPV16、18型感染很普遍,沒有明顯的地區差異,有些HPV型別有地理位置的差異。中國HPV感染型別中52和58型檢出率較高。在台灣進行的一項研究也表明,52和58型較常見。HPV45型在非洲西部宮頸癌組織中很常見,而HPV39和59型僅在美洲的中部和南部宮頸癌組織中出現。
HPV感染生殖道是一個長期的過程,可潛伏在細胞內若干年,一旦機體免疫力降低,潛伏的病毒可恢復活動。HPV感染過程通常分為潛伏感染期、亞臨床感染期、臨床症狀期和HPV相關的腫瘤期。宮頸癌也有一系列的前驅病變,即宮頸上皮不典型增生,在病理上稱宮頸上皮內瘤變(CIN),通常又根據嚴重程度分成三級:宮頸上皮內輕度瘤變(CINI)、宮頸上皮內中度瘤變(CINII)和宮頸上皮內高度瘤變(CINIII),這些癌前病變均有可能發展為宮頸浸潤癌。
在某些自然的或實驗條件下,HPV病毒誘發的乳頭狀瘤雖具有轉化為鱗狀上皮細胞癌的傾向,然而並不是所有的HPV感染者和CIN都會進展為癌。對於大多數乳頭狀瘤,這種轉化還需要其它輔助因子的存在,例如吸菸、化學物質、宿主因素(例如HIV感染)和環境協同因素等,均對疣、乳頭狀瘤轉為惡性腫瘤有致突變及啟動作用。有學者提出了HPV與HSV協同作用誘發宮頸亞性轉化的假說:特異性乳頭狀瘤病毒感染正常細胞導致乳頭狀瘤細胞增生,在HSV感染的啟動下,引起宮頸表皮內惡性轉化的發生,最後導致浸潤癌。這一假說還需進一步驗證。
有關HPV感染和CIN對象轉歸的研究有很多。一些前瞻性研究顯示,HPV感染陽性的婦女在2年內有15-28%進展為宮頸鱗狀上皮內病變(SIL),尤其是HPV16和18型感染危險性更高。HPV陽性婦女能否進展到宮頸上皮內高度病變和癌症,與HPV的型別有很大聯繫。有研究顯示在宮頸低度病變的婦女中,高危型別HPV感染陽性的婦女宮頸病變進展的危險性大於低危型HPV感染或HPV陰性的婦女。此外,HPVDNA劑量水平、HPV首次感染的時間等也很重要。
總之,生殖道HPV感染是一種常見的性傳播疾病。性活躍婦女可能有50%感染過至少一種型別的HPV。由於HPV感染是宮頸癌的病因,因此必須重視這種感染,加強HPV病毒疫苗的研製,消除其對人類的危害。
機理探討
雖沒有研究資料證實依曲替酸有直接抗HPV作用,但很多文獻報告認為口服依曲替酸或依曲替酯對多發、巨大疣有顯著療效。依曲替酸可能通過以下機制發揮對疣治療作用。
1、依曲替酸具有調節表皮細胞分化和增殖作用:抑制表皮細胞的終末分化,縮小表皮細胞的體積。改變角元蛋白的合成方式,抑制細胞膜的形成,影響膜蛋白的合成。能減少表皮細胞角蛋白前身物的量,並使橋粒縮小、發育不良,從而減弱角層細胞粘著力,使角質變薄而抑制角化。經數周治療後,表皮可恢復正常,出現正常角化的上皮,輕度棘層肥厚,細胞內張力微絲、細胞間橋、角化小粒均恢復正常。
2、依曲替酸具有抗增生、抗腫瘤的作用:可中止、抑制、甚至可使癌細胞逆轉。可抑制作為腫瘤發展特徵的鳥氨酸脫羧酶的活性(此酶參與生成聚胺)。還可直接抑制化學致癌物的活性,增強生理性自身修復能力。通過進入細胞,在細胞內與受體結合,形成維甲酸—受體複合物,這種複合物又與DNA中的特異性因子結合,通過靶基因表達,從而修飾分化過程,優先允許正常表皮分化,抑制發育異常的表皮細胞。使惡性腫瘤細胞轉化成較成熟細胞。
3、依曲替酸具有調節免疫作用:能使皮損中已減少的朗格漢細胞數目增加; 激活巨噬細胞; 輔助抗體產生;增強同種異體排斥反應。