分子結構
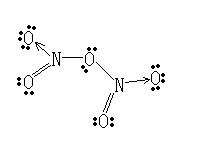 N2O5的結構
N2O5的結構五氧化二氮分子是平面形分子,分子中存在離域π鍵。
五氧化二氮分子中主要為sp2雜化,含有6個σ鍵和2個三原子四電子離域π鍵。因此圖中四個氧原子(除了中間那個以外)實際上是等價的。一般地,在標況下,五氧化二氮為無色固體,在漫射光和280K以下穩定,在氣態時不穩定。
通常認為,固體狀態下,他由兩種離子構成:NO(硝醯陽離子)和 NO(硝酸根離子),其中陽離子呈直線型,鍵長115pm,陰離子呈三角形,鍵長122pm,陰陽離子的中心N原子間距為273pm,且陽離子垂直於陰離子所在平面。這種物質稱為硝酸硝鎓。
毒性
五氧化二氮很容易潮解,而且在10℃以上能分解生成毒氣二氧化氮及氧氣,但在-10℃以下時較穩定。遇高溫及易燃物品,會引起燃燒爆炸。由五氧化二氮引起的火災,可使用水或泡沫進行撲滅。且五氧化二氮屬強氧化劑,與水反應生成強酸。
用途
用作硝化劑、氧化劑。
製法原理
2NO₂+O₃=N₂O₅+O₂
用十氧化四磷(習慣上稱五氧化二磷)使硝酸脫水可得:4HNO+P₄O₁₀=2NO+4HPO3
無機氮化合物
氨 | 聯氨 | 三氟化氮 | 三氯化氮 | 氧氯化氮 | 一氧化二氮 | 一氧化氮 | 三氧化二氮 | 二氧化氮 | 四氧化二氮 | 五氧化二氮 | 亞硝酸 | 連二亞硝酸 | 亞硝酸 | 過氧亞硝酸 | 硝酸 | 過硝酸

