概述
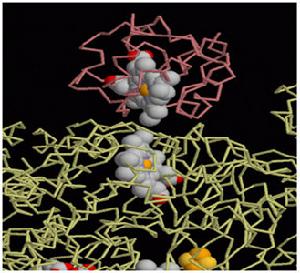 生物無機化學
生物無機化學研究方向
生物無機化學醞釀於20世紀50年代,誕生於60年代。在短短的半個世紀有了很大發展。回顧這段歷史對於人們今後如何開展生命科學中的化學問題研究頗有啟發。早在化學與生物學融合而又分化出生物化學的時候,就孕育著從生物化學中再分化的問題。
生物化學研究的對象是各種生物功能分子,生物學家多注意功能,但是化學進入這個領域之後,注意結構與功能的關係。當時最為直接的結構測定方法是x-射線晶體結構分析,而獲得生物大分子單晶是一個難題。當Perutz因其對肌紅蛋白和血紅蛋白的結構和作用機理研究而獲得諾貝爾化學獎時生物無機化學就開始萌芽。於是在生物化學和結構化學之間開始結合,產生了一個以測定生物功能分子結構和闡明作用機理為內容的新領域。
與此同時,在生物化學深入到涉及金屬離子的生物過程時,必然地與當時正在迅速發展起來的配位化學結合。原來研究溶液配位化學的主要學者均紛紛研究生物配體和金屬離子的溶液化學。R.J.P.Williams,nD.Perrin,K.B.Yatzimirskh,D.R.Williams等等先後進人這個領域,使之成為生物無機化學的另外一個分支。
到後來人們認為,晶體結構與生物介質中的結構未必相同,應該研究溶液中的結構和構象。恰在此時,核磁共振技術大發展,為研究生物大分子的溶液結構創造了條件。於是開拓了結構化學和溶液化學結合、探索含金屬生物大分子結構與功能關係的新領域。生物無機化學的另外一個分支是通過合成模型化合物或結構修飾研究結構-機理關係,它是合成化學介人生物無機化學的結果。這三個分支構成了延續30多年的生物無機化學的主流。雖然研究思路和方法有所改變,但是這些研究都是以認識含無機元素的生物功能分子的結構和功能關係為目的,大都採取分離出單一生物分子,測定其結構,研究有關反應機理以及結構與功能關係的研究模式。雖然這樣的研究取得了許多重要成果,使人們對必需元素和含它們的生物分子認識更加深入。但是近幾年來,這種傳統生物無機化學研究受到一系列實際問題的挑戰。
歸結起來,這些實際問題大都涉及無機物的生物效應,或者說生物體對無機物的應答問題。例如無機藥物的作用機理,無機物中毒機理、環境物質和能損傷生物體的機理等。在這類問題的研究中,共同的核心問題是從分子、細胞到整體三個層次回答構成藥理、毒理作用的基本化學反應和這些反應引起的生物事件。這類研究促使人們把生物無機化學提高到細胞層次,去研究細胞和無機物作用時細胞內外發生的化學變化。這些化學變化是生物效應的基礎。
不可忽視生物無機化學半個世紀的發展對無機化學的啟發和推動作用。例如,混合配體配合物化學、多金屬多配體體系的化學、金屬的異常價態、金屬-硫簇化學、分子內和分子間電子傳遞、自由基化學等等。顯然生物無機化學在未來既可以推動生物學發展,也可以促進化學向新的層次開拓。
發展歷程
1970年,在美國Virginia州舉行了國際生物無機化學討論會,僅19篇報告,並由R.F.Gould彙編“生物無機化學”。
1971年,美國著名化學家G.N.Schrazer主編的雜誌BioinorganicChemistry創刊,1979年更名為J.InorganicBioChemistry
1995年,C.D.Garner和I.Betini再次發起成立國際生物無機化學學會(TheSocietyofBiologicalInorganicChemistry)並於1996年出版會刊“J.ofBiologicalInorganicChemistry”JBIC僅僅幾年時間該刊已躍居國際上最有影響的刊物之一。
1983年起,由I.Bertini,H.B.Gray,B.G.MalmstromandH.Sigel組成生物無機化學國際會議組織委員會,決定每兩年召開一次會議。
Advancesinbioinorganicchemistrysincethe1970shavebeendrivenbythreefactors:
*Rapiddeterminationofhigh-resolutionstructureofproteinsandotherbiomolecules;
*Utilizationofpowerfulspectroscopictoolsforstudiesofbothstructuresanddynamics;
*Thewidespreaduseofmacromolecularengineeringtocreatenewbiologicallyrelevantstructures.Today,verylargemoleculescanbemanipulated,withtheresultthatcertainproteinsandnucleicacidsthemselveshavebecomeversatilemodelsystemsforelucidatingbiologicalfunction.
中國發展
生物無機化學的蘊生和發展差不多經歷了半個世紀,而作為一個獨立學科的建立,卻是1969年以來的事情,通常人們把國際期刊JournalofInorganicBiochemistry的創立(1971年)作為標誌。眾所周知,這個學科是在無機化學和生物學的相互交叉、滲透中發展起來的一門邊沿學科。它的基本任務是從現象學上以及從分子、原子水平上研究金屬與生物配體之間的相互作用。而對這種相互作用的闡明有賴於無機化學和生物學兩門學科水平的高度發展。由於套用理論化學方法和近代物理實驗方法研究物質(包括生物分子)的結構、構象和分子能級的飛速進展,使得揭示生命過程中的生物無機化學行為成為可能,生物無機化學正是這個時候作為一門獨立學科應運而生。
生物無機化學在中國較早就有一些不同學科的研究者在如生物礦化等方面開展工作;但是作為一門學科的出現,似應以全國第一次生物無機化學會議(1984年,武漢)的召開為標誌。總之,從80年代初,中國從事不同學科的化學家順應國際上這一新學科的發展,不少人紛紛轉到生物無機這塊園地進行耕耘。
研究熱點
·金屬蛋白和金屬酶的結構和性質
·金屬離子及其配合物與生物大分子的作用
研究金屬作為DNA探針,與DNA定位結合,DNA定位切割—金屬核酸酶
DNA分子光開關
基因晶片
DNA生物感測器
DNA計算機
·生物礦物
·電子傳遞反應
生命過程的核心問題之一是能量轉換(如呼吸和光合作用),而能量轉換的中心過程是電子傳遞,因此在蛋白質和核酸介質中長程電子傳遞(long-rangeelectrontransfer)是近幾年來生物無機化學研究的熱門課題之一。
·DNA究竟是一根分子導線還是絕緣體,是邇來激烈爭論的焦點。
類型
 生物無機化學
生物無機化學為一類含金屬元素的蛋白:
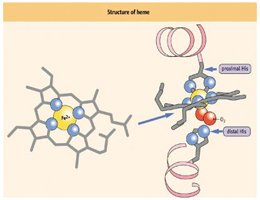
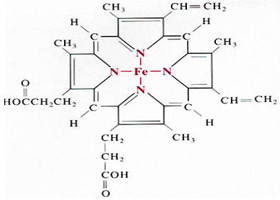
①含鐵蛋白有血紅蛋白、肌紅蛋白、細胞色素C等,其中鐵除與卟啉結合成血紅素基外(見金屬卟啉),並與蛋白質鏈上某一個或兩個胺基酸連線。血紅蛋白和肌紅蛋白分子中的血紅素鐵只與蛋白質鏈上一個組氨酸相連,尚有一個空的配位位置,能可逆地結合一個氧分子,具有運載和貯存氧分子的功能。細胞色素C中血紅素基的鐵原子與蛋白鏈上兩個胺基酸殘基相連,無載氧能力,是重要的電子傳遞體。
② 藍銅蛋白是含銅的重要金屬蛋白,其中銅僅與蛋白鏈上的胺基酸殘基相結合,形成扭曲的四面體構型,呈顯著的藍色,如血漿藍銅蛋白和質體藍素,前者參與調節組織中銅的含量,後者是一系列生物過程中的重要電子傳遞體。
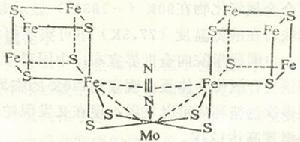
③ 鐵硫蛋白是含鐵、 硫原子的天然原子簇金屬化合物與蛋白質鏈上半胱氨酸結合的金屬蛋白,如植物型鐵氧還蛋白是含Fe2S2原子簇的金屬蛋白,其中每個鐵原子分別與蛋白質鏈上兩個半胱氨酸相連;細菌鐵氧還蛋白含有Fe4S4原子簇,每個鐵原子分別與蛋白質鏈上一個半胱氨酸相連。鐵硫蛋白是生物體中重要的電子傳遞體,如鐵氧還蛋白在葉綠體的光合作用和固氮酶的固氮過程中起傳遞電子的作用。
 生物無機化學
生物無機化學許多金屬蛋白能催化體內的化學反應,是生物體中的催化劑。金屬原子與蛋白質結合較強的稱金屬酶,較弱的稱金屬激活酶。金屬酶中金屬原子常是活性中心的組成部分,如羧肽酶和碳酸酐酶都是鋅酶,前者能催化肽和蛋白質分子羧端胺基酸的水解,後者能催化體內代謝產生的二氧化碳的水合反應。一系列的金屬酶還含其他金屬離子,許多氧化還原酶含價態可變的鐵、銅、鉬、鈷等過渡金屬元素,如固氮酶是含鐵、鉬原子的酶,由鐵蛋白和鐵鉬蛋白組成,在生物體中能催化氮合成氨的反應。
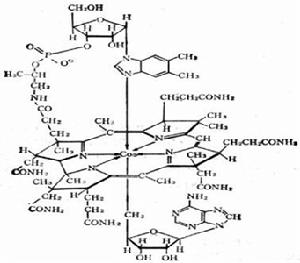
維生素B12和B12輔酶
維生素B12是鈷原子和可啉的配位化合物,鈷原子與可啉環中四個氮原子結合,在軸向又與連結於可啉環的一個核苷酸的苯並咪唑基相連,此外還與一個氰根配位。當氰根被另一個腺苷基代替時,即為B12輔酶。B12對機體的正常生長和營養、細胞和紅細胞的生成以及神經骨髓系統的功能有重要作用。B12的生理功能均以輔酶形式實現。
葉綠素
具有類似於卟啉環的結構,含有鎂原子,其中鎂與環的四個氮原子結合。在植物光合作用中,葉綠素能起將光能轉變為化學能的作用。
離子載體
為一類能與鹼金屬、鹼土金屬等元素結合,生成脂溶性配位化合物,從而增大金屬離子透過生物膜可能性的物質。離子載體有天然和合成的兩種:天然離子載體如纈氨酶素等,能使正常情況下不易通過線粒體內膜的鉀離子得以順利通過;合成的離子載體主要為冠醚,如二苯並18-冠-6為環狀多醚,其中央空穴的大小,決定與金屬離子配位的選擇性。二苯並18-冠-6的鹼金屬配位化合物的穩定性有以下次序:K+ >Na+ >Cs+ >Li+ 。
研究方法
 生物無機化學
生物無機化學含金屬元素的生物無機化合物的功能常能用較簡單的金屬配合物或類似物來模擬,此種化合物稱模型化合物。模型化合物常具有被模擬體系的結構特點或有一定的有關生物活性。通過模型化合物的研究,常能了解複雜的被模擬體系的結構與其功能間的關係。例如,曾合成一系列籬笆式、帽式、尾巴鹼式的血紅素,它們並無肽鏈,但能像血紅蛋白、肌紅蛋白一樣可逆地結合和放出氧分子。通過模型化合物的研究,了解到血紅素必須存在於疏水環境中,周圍的位阻效應是保證血紅蛋白、肌紅蛋白可逆結合氧分子的條件,而其中的二價鐵必須具有不被氧化成三價的必要結構因素。又如,通過對一系列銅與多肽配位化合物的結構和性質研究,了解到藍銅蛋白分子中銅原子周圍有扭曲的四面體配位,使藍銅蛋白具有顯著的藍色和高的還原電勢。模擬體系與天然體系總有差別,用模擬體系的研究結果來說明天然體系的結構、功能和機理時必須謹慎。
無機離子生物探針:用一些其他的金屬元素替代生物無機化合物中的原有金屬元素,從而用各種波譜方法來研究和確定體系的結構和作用。所用的金屬離子稱生物探針。用作探針的金屬離子應與原有離子有相近的半徑,並能保持原有體系的結構特點和一定的生物活性。例如,用半徑與鋅相近的鈷離子作探針,代替羧肽酶中的鋅,從而根據含鈷酶的光譜推斷羧肽酶中鋅的配位環境;用錳離子做探針,根據含錳羧肽酶的核磁共振譜確定了羧肽酶中鋅和一水分子或羥基相連。
 生物無機化學
生物無機化學在生物體中金屬離子尚有許多重要的生理功能。金屬離子參與細胞分裂、肌肉收縮、神經脈衝的傳遞等過程。金屬離子對維持細胞壁結構、對脂蛋白膜加固有重要作用;金屬離子還直接影響核糖體的結構,從而影響蛋白質的正常合成過程。
體內金屬離子的種類及濃度失調,將影響正常的生命活動,如體內缺乏鐵、銅、鈷會引起貧血;鎘離子過量與心血管病的發病有關;硒過量對肌體有毒,但過低能引起病毒誘發癌;先天性銅代謝障礙能引起威爾遜氏病。
為控制體內金屬元素的正常含量,常用一些金屬螯合劑(見螯合作用)來排除體內過量的金屬元素。例如,1、2-二巰基丙醇可排除汞、鉛、銻等元素;EDTA(乙二胺四乙酸)可排除多種有害元素及過量金屬;青黴胺可治療威爾遜氏病等等。某些金屬配合物具有殺菌、抗病毒和抗癌等生物活性。其中順式 -二氯二氨合鉑對生殖泌尿系統癌有較好療效,它能抑制癌細胞中DNA(脫氧核糖核酸)的複製。
中國發展
 生物無機化學
生物無機化學生物無機化學在中國較早就有一些不同學科的研究者在如生物礦化等方面開展工作;但是作為一門學科的出現,似應以全國第一次生物無機化學會議(1984年,武漢)的召開為標誌。總之,從80年代初,中國從事不同學科的化學家順應國際上這一新學科的發展,不少人紛紛轉到生物無機這塊園地進行耕耘。
![生物無機化學[自然科學門類] 生物無機化學[自然科學門類]](/img/5/002/nBnauM3XzITM2ADNwETOyUDN3QTM3IDO1gzMxADMwAzMwIzLxkzL2MzLt92YucmbvRWdo5Cd0FmLyE2LvoDc0RHa.jpg)
