分子結構
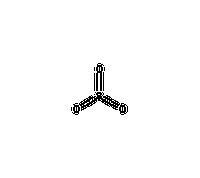 三氧化硫
三氧化硫基本內容
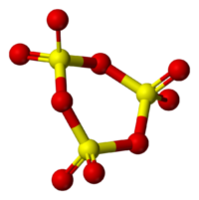 三氧化硫
三氧化硫中文名稱:三氧化硫
英文名稱:sulfur trioxide
中文別名:硫酸酐(液);硫酸酐;三氧化硫(禁運);三氧化硫(液)
英文別名:SO3; Sulfan; Sulfur oxide (SO3); Sulfur trioxide, stabilized; Sulfuric oxide; Sulfuricacidanhydride; sulfuricoxide; sulfurtrioxide,stabilized
CAS號:7446-11-9
分子式:SO3
分子量:80.06
物性數據
1. 性狀:無色透明油狀液體,具有強刺激性臭味。
2. 密度(g/mL,25/4℃): 1.92 g/cm3
3. 相對蒸汽密度(g/mL,空氣=1):2.8
4. 熔點(ºC):16.9 °C, 62.4 °F
5. 沸點(ºC,常壓):45 °C, 113 °F
6. 沸點(ºC,5.2kPa): 無可用
7. 折射率: 無可用
8. 閃點(ºC): 非易燃
9. 比鏇光度(º):無可用
10. 自燃點或引燃溫度(ºC):無可用
11. 蒸氣壓(kPa,25ºC):280 mm Hg
12. 飽和蒸氣壓(kPa,60ºC):無可用
13. 燃燒熱(KJ/mol):256.77 J·K−1·mol−1
14. 臨界溫度(ºC):無可用
15. 臨界壓力(KPa):無可用
16. 油水(辛醇/水)分配係數的對數值:無可用
17. 爆炸上限(%,V/V):無可用
18. 爆炸下限(%,V/V): 無可用
19. 溶解性:溶於水,於水反應
存儲方法
密封於常壓陰涼(45ºC以下)的乾燥環境,切勿與水接觸,否則會形成硫酸!
合成方法
發煙硫酸法將硫黃(或硫鐵礦或其他含硫物質)與乾燥空氣在焚硫爐內燃燒,生成高濃度二氧化硫氣體,經催化氧化生成三氧化硫,用硫酸吸收製得發煙硫酸,再經蒸餾得到三氧化硫氣體,經冷卻、壓縮液化,製得液體三氧化硫成品。其
物品簡介
三氧化硫是一種硫的氧化物,分子式為SO3,是非極性分子。它的氣體形式是一種嚴重的污染物,是形成酸雨的主要來源之一。
常溫下為無色透明油狀液體或固體(取決於具體晶型),標況為固體,具有強刺激性臭味。相對密度1.97(20℃)。熔點16.83℃(289.8K)。沸點44.8℃(101.3kPa、317.8K)。強氧化劑,能被硫、磷、碳還原。較硫酸、發煙硫酸的脫水作用更強。對金屬的腐蝕性比硫酸、發煙硫酸弱。
成鍵方式
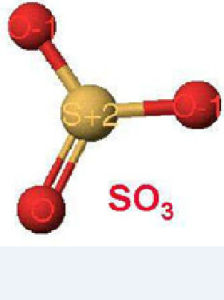
SO3中,S元素採取sp2雜化,在豎直方向(就是沒形成雜化軌道剩下的p軌道)上的p軌道中有一對電子,在形成的雜化軌道中有一對成對電子和2個成單電子,有2個氧原子分別與其形成σ鍵,2個氧原子豎直方向上p軌道各有1個電子,一個氧原子與雜化軌道的孤對電子形成配位鍵,其豎直方向上有2個電子,這樣,在4個原子的豎直方向的電子共同形成一套四中心六電子大π鍵,這套大π鍵是離域的鍵。
分子構型
氣態的SO3是一種具有D3h對稱的平面正三角形分子,這與價層電子對互斥理論(VSEPR)所預測的結論是一致的。
三氧化硫中,硫元素的化合價為+6,分子為非極性分子。
SO3分子中的S已經達到+6價,所有的電子都參與成鍵,沒有孤對電子,不需要給孤對電子留出空間了,所以它是很對稱的平面正三角形。
與二氧化硫一樣都是硫的氧化物。
化學反應
SO是硫酸(HSO)的酸酐。因此,可以發生以下反應:
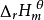 三氧化硫
三氧化硫和水化合成硫酸:SO(l) + HO(l) = HSO(aq) (
=-88 kJ/mol)
這個反應進行得非常迅速,而且是放熱反應。在大約340 ℃以上時,硫酸、三氧化硫和水才可以在平衡濃度下共存。
三氧化硫也與二氯化硫發生反應來生產很有用的試劑——亞硫醯氯:
SO+ SCl →SOCl + SO
三氧化硫還可以與鹼類發生反應,生成硫酸鹽及其它物質,如:SO+2NaOH=NaSO+HO
三氧化硫不可用濃硫酸乾燥,因為SO3和濃硫酸會生成焦硫酸:
HSO+SO=HSO
二氧化硫可轉為三氧化硫:
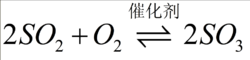 三氧化硫
三氧化硫固態結構
天然的SO3固體有一種令人驚訝的、因痕量水導致結構改變的複雜結構。由於氣體的液化,極純的SO3冷凝形成一種通常稱作γ-SO3的三聚體。這種分子形式是一種熔點在16.8°C的無色固體。它形成的環狀結構被稱為[S(=O)(μ-O)]3。
如果SO3在27°C以上冷凝,可形成熔點為16.83°C的"α-SO3".α-SO3外觀為類似石棉的纖維狀(雖然兩者相差甚遠)。在結構上來說,它是形如[S(=O)2(μ-O)]n的聚合物。聚合物分子的每個末端都以-OH結束。β-SO3是與α構型相類似、但相對分子質量不同的纖維狀聚合物,其分子末端亦皆為羥基,熔點為62.4°C。γ構型和β構型都是介穩的,在長時間放置後最終會轉化為穩定的α構型。這種轉化是由痕量水導致的。
 三氧化硫
三氧化硫在同一溫度下固體SO3的相對蒸氣壓大小為α<β><γ,亦指明它們相對分子質量的大小。液態三氧化硫的蒸氣壓說明它是γ構型。因此加熱α-SO3的晶體至其熔點時會導致蒸氣壓的突然升高,巨大的壓力甚至可以衝破加熱它的玻璃管。這個結果被稱為"α爆炸"。SO3極易水解。事實上,該水化熱足以使混合了SO3的木頭或者棉花點燃。在這種情況下,SO3使那些碳水化合物脫水。>
SO3中氧硫鍵的鍵長並不相同,固態SO3主要以兩種形式存在:一種是三聚體的環狀形式,另外一種是石棉鏈狀的纖維結構兩種結構中,共享的S—O鍵長和非共享的S—O鍵長是不同的。
製備
實驗室製法
在實驗室中常用濃硫酸與五氧化二磷共熱製取三氧化硫,其中會產生磷酸。在反應中生成的三氧化硫需要用冰水混合物冷卻,尾氣用濃硫酸(85%)吸收。
工業製法
SO3的工業製法是接觸法。二氧化硫通常通過硫的燃燒或黃鐵礦礦石(一種含硫鐵礦石,主要成分二硫化亞鐵FeS2)的煅燒得到的,先通過靜電沉澱進行提純。提純後的SO2在400至600°C的溫度下,用負載在硅藻土上的含氧化鉀或硫酸鉀(助催化劑)的五氧化二釩作為催化劑,將二氧化硫用氧氣氧化為三氧化硫。鉑同樣可以充當這個反應的催化劑但是價格昂貴,比混合物更容易發生催化劑中毒(導致失效)。以這種方式製得的三氧化硫大部分都被轉化為了硫酸,但不能用水進行吸收,否則將形成大量酸霧,但如果採用98.3%硫酸作吸收劑,因其液面上水、三氧化硫和硫酸的總蒸氣壓最低,故吸收效率最高。
化學產品
一化學品名及成分
化學品中文名稱:三氧化硫
化學品英文名稱:sulphurtrioxide
中文名稱2:硫酸酐
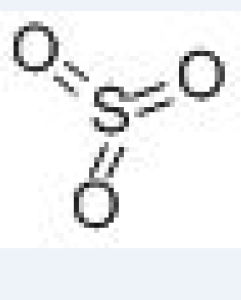 三氧化硫結構分子式
三氧化硫結構分子式英文名稱2:Sulfuricanhydride
技術說明書編碼:1236
CASNo.:7446-11-9
EINECS號:231-197-3
InChI:InChI=1/O3S/c1-4⑵3
分子式:SO3
分子量:80.06
分子結構:S原子以sp2雜化軌道成鍵,分子為平面正三角形分子。
有害物成分CASNo.
三氧化硫7446-11-9
二危險性概述
侵入途徑:
健康危害:其毒性表現與硫酸相同。對皮膚、黏膜等組織有強烈的刺激和腐蝕作用。可引起結膜炎、水腫。角膜混濁,以致失明;引起呼吸道刺激症狀,重者發生呼吸困難和肺水腫;高濃度引起喉痙攣或聲門水腫而死亡。口服後引起消化道的燒傷以至潰瘍形成。嚴重者可能有胃穿孔、腹膜炎、喉痙攣和聲門水腫、腎損害、休克等。慢性影響有牙齒酸蝕症、慢性支氣管炎、肺氣腫和肝硬變等。
環境危害:對環境有危害,對大氣可造成污染。
燃爆危險:該品不燃,具強腐蝕性、強刺激性,可致人體灼傷。
三應急處理
皮膚接觸:立即脫去污染的衣著並迅速擦淨接觸部分,之後用大量流動清水沖洗至少15分鐘。就醫。
眼睛接觸:立即提起眼瞼,用大量流動清水或生理鹽水徹底沖洗至少15分鐘。就醫。
吸入:迅速脫離現場至空氣新鮮處。保持呼吸道通暢。如呼吸困難,給輸氧。如呼吸停止,立即進行人工呼吸。就醫。
食入:用水漱口,給飲牛奶或蛋清。就醫。
危險特性:與水發生爆炸性劇烈反應。與氟、氧化鉛、次氯酸、亞氯酸、高氯酸、磷、四氟乙烯等接觸劇烈反應。與有機材料如木、棉花或草接觸,會著火。吸濕性極強,在空氣中產生有毒的白霧。遇潮時對大多數金屬有強腐蝕性。
有害燃燒產物:硫氧化物。
滅火方法:該品不燃。消防人員必須佩戴過濾式防毒面具(全面罩)或隔離式呼吸器、穿全身防火防毒服,在上風向滅火。儘可能將容器從火場移至空曠處。噴水保持火場容器冷卻,直至滅火結束。滅火時儘量切斷泄漏源,然後根據著火原因選擇適當滅火劑滅火。禁止用水和泡沫滅火。
泄漏應急處理:迅速撤離泄漏污染區人員至安全區,並立即隔離150m,嚴格限制出入。建議應急處理人員戴自給正壓式呼吸器,穿防酸鹼工作服。儘可能切斷泄漏源。若是液體。小量泄漏:用砂土、蛭石或其它惰性材料吸收。大量泄漏:構築圍堤或挖坑收容。用泵轉移至槽車或專用收集器內,回收或運至廢物處理場所處置。若是固體,用潔淨的鏟子收集於乾燥、潔淨、有蓋的容器中。若大量泄漏,收集回收或運至廢物處理場所處置。
四操作處置與儲存
操作注意事項:密閉操作,注意通風。操作儘可能機械化、自動化。操作人員必須經過專門培訓,嚴格遵守操作規程。建議操作人員佩戴防塵面具(全面罩),穿橡膠耐酸鹼服,戴橡膠耐酸鹼手套。遠離易燃、可燃物。避免與還原劑、鹼類、活性金屬粉末接觸。尤其要注意避免與水接觸。搬運時要輕裝輕卸,防止包裝及容器損壞。配備泄漏應急處理設備。倒空的容器可能殘留有害物。
儲存注意事項:儲存於陰涼、乾燥、通風良好的庫房。遠離火種、熱源。保持容器密封。應與易(可)燃物、還原劑、鹼類、活性金屬粉末等分開存放,切忌混儲。儲區應備有泄漏應急處理設備和合適的收容材料。
五操作處置與儲存
職業接觸限值
中國PC-TWA(mg/m3):1
PC-STEL(mg/m3):2
前蘇聯MAC(mg/m3):1
TLVTN:未制定標準
TLVWN:未制定標準
監測方法:氯化鋇比濁法
工程控制:密閉操作,注意通風。儘可能機械化、自動化。提供安全淋浴和洗眼設備。
呼吸系統防護:可能接觸其粉塵時,必須佩戴防塵面具(全面罩);可能接觸其蒸氣時,應該佩戴自吸過濾式防毒面具(全面罩)。
眼睛防護:呼吸系統防護中已作防護。
身體防護:穿橡膠耐酸鹼服。
手防護:戴橡膠耐酸鹼手套。
其他防護:工作完畢,淋浴更衣。單獨存放被毒物污染的衣服,洗後備用。保持良好的衛生習慣
六理化特徵
主要成分:純品
外觀與性狀:針狀固體或液體,有刺激性氣味。
熔點(℃):16.8
沸點(℃):44.8
相對密度(水=1):1.97
相對蒸氣密度(空氣=1):2.8
飽和蒸氣壓(kPa):37.32/25℃
燃燒熱(kJ/mol):無意義
臨界溫度(℃):無資料
臨界壓力(MPa):無資料
辛醇/水分配係數的對數值:無資料
閃點(℃):無意義
引燃溫度(℃):無意義
爆炸上限%(V/V):無意義
爆炸下限%(V/V):無意義
溶解性:劇烈反應
主要用途:有機合成用磺化劑。
其它理化性質:暫無
七穩定性和反應活性
穩定性:暫無
禁配物:強鹼、強還原劑、活性金屬粉末、水、易燃或可燃物。
避免接觸的條件:潮濕空氣。
聚合危害:暫無
分解產物:暫無
八生態、毒理學
急性毒性:LD50:無資料
LC50:無資料
亞急性和慢性毒性:暫無
刺激性:暫無
致敏性:暫無
致突變性:暫無
致畸性:暫無
致癌性:暫無
生態毒理毒性:暫無
生物降解性:暫無
非生物降解性:暫無
生物富集或生物積累性:暫無
其它有害作用:該物質對環境有危害,應特別注意對大氣的污染。有造成酸雨的危害
九廢棄處置
廢棄物性質:暫無
廢棄處置方法:根據國家和地方有關法規的要求處置。或與廠商或製造商聯繫,確定處置方法。
廢棄注意事項:暫無
十運輸、法規信息
危險貨物編號:81010
UN編號:1829
包裝標誌:暫無
包裝類別:暫無
包裝方法:特製金屬容器,外用堅固木箱;耐酸壇或陶瓷瓶外普通木箱或半花格木箱;磨砂口玻璃瓶或螺紋口玻璃瓶外普通木箱。
運輸注意事項:鐵路運輸時應嚴格按照鐵道部《危險貨物運輸規則》中的危險貨物配裝表進行配裝。起運時包裝要完整,裝載應穩妥。運輸過程中要確保容器不泄漏、不倒塌、不墜落、不損壞。嚴禁與易燃物或可燃物、還原劑、鹼類、活性金屬粉末、食用化學品等混裝混運。運輸時運輸車輛應配備泄漏應急處理設備。運輸途中應防曝曬、雨淋,防高溫。公路運輸時要按規定路線行駛,勿在居民區和人口稠密區停留。
法規信息化學危險物品安全管理條例(1987年2月17日國務院發布),化學危險物品安全管理條例實施細則(化勞發677號),工作場所安全使用化學品規定(勞部發423號)等法規,針對化學危險品的安全使用、生產、儲存、運輸、裝卸等方面均作了相應規定;常用危險化學品的分類及標誌(GB13690-92)將該物質劃為第8.1類酸性腐蝕品。
安全信息
風險術語
R14:Reacts violently with water. 遇水反應劇烈。
R34:Causes burns. 引起灼傷。
安全術語
S25:Avoid contact with eyes. 避免眼睛接觸。
S36/37/39:Wear suitable protective clothing, gloves and eye/face protection.穿戴適當的防護服、手套和護目鏡或面具。
S45:In case of accident or if you feel unwell, seek medical advice immediately (show the label whenever possible.)
若發生事故或感不適,立即就醫(可能的話,出示其標籤)。
S8:Keep container dry. 保持容器乾燥。
系統編號
CAS號:7446-11-9
MDL號:MFCD00011452
EINECS號:231-197-3
RTECS號:WT4830000
PubChem號:24866637
毒理學數據
1 。 試驗方法:吸入攝入劑量: 30 mg/m3 測試對象:人力毒性類型:急性毒性作用: 1.感官(嗅覺)異常2.肺 ,胸部或呼吸-咳嗽3.肺 ,胸部或呼吸-其他變化2 。 試驗方法:吸入攝入劑量: 30 mg/m3/6H 測試對象:齧齒動物-豚鼠毒性類型:急性毒性作用: 1.肝臟 -肝炎(肝細胞壞死) ,瀰漫性2.肺,胸部或呼吸-結構或功能改變,氣管或支氣管3.其他變化
分子結構數據
1、 摩爾折射率:13.02
2、 摩爾體積(m3/mol):35.1
3、 等張比容(90.2K):131.3
4、 表面張力(dyne/cm):194.2
5、 極化率(10-24cm3):5.16
計算化學數據
1、 疏水參數計算參考值(XlogP):-0.5
2、 氫鍵供體數量:0
3、 氫鍵受體數量:3
4、 可鏇轉化學鍵數量:0
5、 拓撲分子極性表面積(TPSA):51.2
6、 重原子數量:4
7、 表面電荷:0
8、 複雜度:61.8
9、 同位素原子數量:0
10、 確定原子立構中心數量:0
11、 不確定原子立構中心數量:0
12、 確定化學鍵立構中心數量:0
13、 不確定化學鍵立構中心數量:0
14、 共價鍵單元數量:1
生態學數據
該物質對環境可能有危害,對水體應給予特別注意。
性質與穩定性
如果遵照規格使用和儲存則不會分解。
三氧化硫的物理性質
純淨的SO3是無色易揮發的固體,熔點289.9K,沸點317.8K,263K時密度為,293K時為。
三氧化硫的化學性質
SO3中S原子處於最高氧化態+6,所以SO3是一種強氧化劑,特別在高溫時它能氧化磷、碘化物和鐵、鋅等金屬:
SO3極易吸收水分,在空氣中強烈冒煙,溶於水即生成硫酸並放出大量熱。

