化學性質
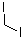 二碘甲烷
二碘甲烷二碘甲烷可以和氯氣發生取代反應。二碘甲烷亦可以和活潑金屬反應。
二碘甲烷受熱後,會分解出有毒的碘化物煙氣。暴露於光線下,會分解出碘,而呈現褐色
分解的產物分別為一氧化碳、二氧化碳以及碘化氫
(參考:Carson, A.S.; Laye, P.G.; Pedley, J.B.; Welsby, A.M., The enthalpies of formation iodomethane, diiodomethane, triiodomethane, and tetraiodomethane by rotating combustion calorimetry, J. Chem. Thermodyn., 1993, 25, 261-269)
基本內容
中文名稱:二碘甲烷
英文名稱:Diiodomethane
別名:4-甲苯基硫脲 對甲基苯基硫脲
更多名稱:4-Tolythiourea p-Methylphenylthiourea 4-Methylphenylthiourea
CAS號:75-11-6
MDL:MFCD00001079
分子式:CH2I2
分子量:267.8355
物性數據
1.性狀:無色澄清至淡黃色液體。
2.熔點(℃):5~6
3.沸點(℃):181(分解)
4.相對密度(水=1):3.32
5.相對蒸氣密度(空氣=1):9.25
6.燃燒熱(kJ/mol):-745.7
7.臨界壓力(MPa):5.47
8.辛醇/水分配係數:2.3
9.閃點(℃):110
10.溶解性:不溶於水,溶於乙醇、乙醚、苯、氯仿等多數有機溶劑。
11.常溫折射率(n20):1.7411
12.常溫折射率(n25):1.7380
13.溶度參數(J·cm-3)0.5:24.055
14.van der Waals面積(cm2·mol⁻¹):6.430×109
15.van der Waals體積(cm3·mol-1):50.930
16.黏度(10ºC):3.35mPa。s
17.液相標準聲稱熱(焓)( kJ·mol-1):67.8
18.液相標準熱熔(J·mol-1·K-1):135.5
19.氣相標準聲稱熱(焓)( kJ·mol-1) :118.7
20.氣相標準熵(J·mol-1·K-1) :309.50
21.氣相標準生成自由能( kJ·mol-1):101.7
22.氣相標準熱熔(J·mol-1·K-1):57.73
存儲方法
儲存注意事項 儲存於陰涼、通風的庫房。遠離火種、熱源。保持容器密封。應與氧化劑、鹼類、鹼金屬、食用化學品分開存放,切忌混儲。配備相應品種和數量的消防器材。儲區應備有泄漏應急處理設備和合適的收容材料。
合成方法
1.碘仿、亞砷酸鈉法首先用三氧化二砷和液鹼反應,配製亞砷酸鈉,然後由碘仿、亞砷酸鈉溶液混合,在攪拌下加熱至60~65℃,再加氫氧化鈉一步反應製取二碘甲烷。反應產物經水洗、蒸餾、脫色、結晶、分離和乾燥,得成品。
2.碘仿法經與醋酸鈉作用而得,其反應式如下:上述反應完成後,經蒸餾得成品。
3.相轉移催化合成法以三乙基苄基氯化銨為催化劑,由二氯甲烷與碘化鈉反應而得,其反應式如下:
主要用途
1.有機合成原料、化學試劑和藥品中間體,可用於製造X光造影劑,測定礦物密度和折射率,以及分離礦物等。2.二碘甲烷是一種亞甲基轉移試劑,可以與不同的金屬或者烷基金屬反應生成卡賓, 與烯烴發生環丙烷化反應,也可以與羰基發生亞甲基化反應。同時也可以製備ICH2M和I2CHM等親核試劑,也能夠參與自由基偶聯反應。亞甲基化 很多的羰基亞甲基化試劑都使用二碘甲烷作為碳源,可以作為Wittig反應的替代方法;在酮存在下,二碘甲烷和鎂汞齊反應,可以得到很高產率的烯烴 (式1)。不同結構的醛和酮都可以發生這個反應。Lewis酸的存在可以極大地加速該反應的進行,提高反應的選擇性和產率。常用的Lewis酸包括三甲基鋁、四異丙氧基鈦、四氯化鈦、二氯二(環戊二烯基)鋯等。其中,CH2I2/Zn/ Me3Al和CH2Br2/Zn/TiCl4兩組試劑的效果最好。在有酮存在的條件下,醛可以選擇性發生亞甲基化反應 (式2)。環丙烷化 在有機合成中,二碘甲烷主要用來進行金屬參與的環丙烷化反應。最重要的是鋅參與的環丙烷化 (Simmons-Smith反應),這是一個被廣泛套用並且能夠實現多種變化的試劑。鋅的來源對反應的成敗至關重要,Zn/Cu、二乙基鋅等都可以作為Zn的來源進行環丙烷化反應。二碘甲烷和釤汞或者碘化釤可以組合得到很多不同的含釤烯烴環丙烷化試劑,這些試劑都能夠和烯丙醇以及烯醇反應。α,β-不飽和酯、α,β-不飽和醯胺也可以在釤催化下與二碘甲烷發生環丙烷化反應 (式3)。含鋅試劑和含釤試劑的環丙烷化反應都受到羥基的直接影響。用三烷基鋁 (如三異丁基鋁) 處理二碘甲烷也會得到相應的環丙烷,這是對鋅和釤體系的一個很好的補充,此反應傾向於和獨立的烯烴反應,而不是與烯丙醇反應 (式4)。‘ICH2’的親核加成 由金屬釤製備的碘甲基鋰可以和醛、酮及烯酮反應,鎂試劑也可以用於這一反應 (式5)。而用鋁試劑還可以實現碘甲基對烯丙醇羥基的取代,Et3Al、Et2AlCl、Et2AlOEt都可以參與這個反應 (如式6)。(+)-trans-(2S,3S)-二(二苯基膦)二環[2.2.1]庚-5-烯‘I2CH’的親核加成 CH2I2在鹼作用下去質子化後得到I2CHM的衍生物,這些化合物比相應的ICH2M更穩定,能夠和許多親電試劑進行反應。常用的鹼有Cy2NLi、NaHMDS、LiHMDS以及LDA等。烯丙基碘就是用I2CHLi來合成的。首先用LiHMDS處理二碘甲烷,然後再加入碸,蒸乾水分之後就可以得到烯丙基碘,但是選擇性相對較差 (式7)。自由基加成 在三乙基硼烷存在的情況下,ICH2碎片與α,β-不飽和酮發生加成反應,得到γ-碘酮 (式8)。中間體烯醇化硼既可以被水解,也可以被烷基化。烷基化反應 二碘甲烷在烷基化方面的套用有限,ClCH2I和ClCH2Br比二碘甲烷更容易發生烷基化反應,但是,二碘甲烷可以用於環烷基化反應中。二胺可以與二碘甲烷反應,緩慢向二胺溶液中加入二碘甲烷溶液可以得到較高的產率 (式9)。在有Pt作為催化劑的反應中,二碘甲烷和硫醇反應可以得到二噻烷。另外,在二碘甲烷與烷基鋰共同存在下原位生成碘甲基鋰,能夠方便快速地將很多羰基化合物轉化為環氧化物 (式10)。3.用於有機合成及混合礦物的分離。
對環境的影響
該物質對環境有危害,應注意對大氣的污染。
健康危害
侵入途徑:吸入、食入、經皮吸收。
健康危害:高濃度時有麻醉和刺激作用。大鼠腹腔注射血中產生碳氧血紅蛋白。
安全術語
S26In case of contact with eyes, rinse immediately with plenty of water and seek medical advice.
不慎與眼睛接觸後,請立即用大量清水沖洗並徵求醫生意見。
S37/39Wear suitable gloves and eye/face protection
戴適當的手套和護目鏡或面具。
風險術語 R36/37/38Irritating to eyes, respiratory system and skin.
刺激眼睛、呼吸系統和皮膚。
毒理學資料及環境行為
急性毒性:LD50403mg/kg(大鼠腑腔內);830mg/kg(小鼠皮下)
危險特性:受熱分解放出有毒的碘化物煙氣。與鋰、鉀鈉合金接觸劇烈反應。
燃燒(分解)產物:一氧化碳、二氧化碳、碘化氫。
基本內容
1.物質的理化常數
國標編號 61569
CAS號 75-11-6
中文名稱 二碘甲烷
英文名稱 diiodomethane;Methylene iodide
別 名 碘化亞甲基
MDL: MFCD00001079
分子式 CH2I2 外觀與性狀 無色澄清到淡黃色液體
分子量 267.87 閃 點 110℃
熔 點 5~6℃ 沸點:181℃/分解 溶解性 不溶於水,溶於乙醇、乙醚、苯、氯仿等多數有機溶劑
密 度 相對密度(水=1)3.32;相對密度(空氣=1)9.25 穩定性 穩定
危險標記 14(有毒品) 主要用途 用於有機合成及混合礦物的分離
重質高折射率黃色液體。溶於約70份水,與乙醇、丙醇、異丙醇、正己烷、環己烷、乙醚、氯仿和苯等溶劑混溶,可溶解硫和磷(25℃時多於1:1),在空氣中易分解,暴露於光、空氣及遇潮濕易變黑。
二碘甲烷的熔點為5.7℃,通常冷至0℃時開始結晶。沸點180℃(分解),106-107℃(9.33kPa),68℃(1.47kPa),相對密度3.3254(20/4℃),折射率1.7425(15℃)。黏度(10℃)3.35mPa·s。
2.對環境的影響
該物質對環境有危害,應注意對大氣的污染。
一、健康危害
侵入途徑:吸入、食入、經皮吸收。
健康危害:高濃度時有麻醉和刺激作用。大鼠腹腔注射血中產生碳氧血紅蛋白。
二、毒理學資料及環境行為
急性毒性:LD50403mg/kg(大鼠腑腔內);830mg/kg(小鼠皮下)
危險特性:受熱分解放出有毒的碘化物煙氣。與鋰、鉀鈉合金接觸劇烈反應。
燃燒(分解)產物:一氧化碳、二氧化碳、碘化氫。
3.現場應急監測方法
4.實驗室監測方法
澱粉比色法《空氣中有害物質的測定方法》(第二版),杭士平主編
5.環境標準
6.應急處理處置方法
一、泄漏應急處理
迅速撤離泄漏污染區人員至安全區,並進行隔離,嚴格限制出入。切斷火源。建議應急處理人員戴自給正壓式呼吸器,穿一般作業工作服。儘可能切斷泄漏源,防止進入下水道、排洪溝等限制性空間。小量泄漏:用砂土、蛭石或其它惰性材料吸收。大量泄漏:構築圍堤或挖坑收容。用泡沫復蓋,降低蒸氣災害。用泵轉移至槽車或專用收集器內,回收或運至廢物處理場所處置。
二、防護措施
呼吸系統防護:一般不需要特殊防護,高濃度接觸時可佩戴自吸過濾式防毒面具(半面罩)。
眼睛防護:必要時,戴安全防護眼鏡。
身體防護:穿透氣型防毒服。
手防護:戴防化學品手套。
其它:工作現場禁止吸菸、進食和飲水。工作畢,沐浴更衣。單獨存放被毒物污染的衣服。洗後備用。注意個人清潔衛生。
三、急救措施
皮膚接觸:脫去被污染的衣著,用肥皂水和清水徹底沖洗皮膚。就醫。
眼睛接觸:提起眼瞼,用流動清水或生理鹽水沖洗,就醫。
吸入:迅速脫離現場至空氣新鮮處。保持呼吸道通暢。如呼吸困難,給輸氧。如呼吸停止,立即進行人工呼吸。就醫。
食入:飲足量溫水,催吐,就醫。
滅火方法:消防人員須佩戴防毒面具、穿全身消防服。滅火劑:霧狀水、泡沫、二氧化碳、砂土。
產品用途
用作分析試劑,也用於有機合成
二碘甲烷還可以作為寶石鑑定的比重液
系統編號
CAS號:75-11-6
MDL號:MFCD00001079
EINECS號:200-841-5
RTECS號:PA8575000
BRN號:1696892
PubChem號:24849735
毒理學數據
1、急性毒性
小孩口服LDLO: 2778 uL/kg
大鼠腹腔LD50: 403mg/kg
小鼠腹腔LD50: 467mg/kg
小鼠皮下LD50: 830mg/kg
2.急性毒性 LD50:403mg/kg(大鼠經口);830mg/kg(大鼠經皮)
3.刺激性 暫無資料
4.致突變性 微生物致突變性:大腸桿菌3mg/皿。
分子結構數據
1、摩爾折射率:32.62
2、摩爾體積(m3/mol):82.6
3、等張比容(90.2K):219.9
4、表面張力(dyne/cm):50.0
5、極化率(10-24cm3):12.93
計算化學數據
1、疏水參數計算參考值(XlogP):2.3
2、氫鍵供體數量:0
3、氫鍵受體數量:0
4、可鏇轉化學鍵數量:0
5、互變異構體數量:
6、拓撲分子極性表面積(TPSA):0
7、重原子數量:3
8、表面電荷:0
9、複雜度:2.8
10、同位素原子數量:0
11、確定原子立構中心數量:0
12、不確定原子立構中心數量:0
13、確定化學鍵立構中心數量:0
14、不確定化學鍵立構中心數量:0
15、共價鍵單元數量:1
生態學數據
1.生態毒性 暫無資料
2.生物降解性 暫無資料
3.非生物降解性 暫無資料
4.其他有害作用 該物質對環境有危害,應注意對大氣的污染。
性質與穩定性
1.有毒。比二溴甲烷的麻醉性弱。
2.嗅後引起頭痛、呼吸困難。參見二溴甲烷。
3.與銅粉存放在一起可以有效地阻止其分解;應注意避光保存;與許多金屬 (如Al、Mg、Na等) 和強鹼不能共存;有一定的腐蝕性;要在通風櫥中進行操作。
4.穩定性穩定
5.禁配物 強氧化劑、強鹼、鹼金屬
6.避免接觸的條件 受熱、光照
7.聚合危害 不聚合
8.分解產物 碘化物
