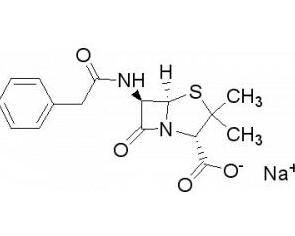
研發歷史
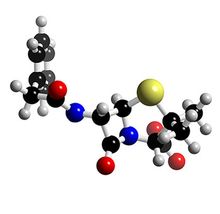 青黴素
青黴素 青黴素是人類歷史上發現的第一種抗生素,且套用非常廣泛。早在唐朝時,長安城的裁縫會把長有綠毛的糨糊塗在被剪刀劃破的手指上來幫助傷口癒合,就是因為綠毛產生的物質(青黴素素菌)有殺菌的作用,也就是人們最早使用青黴素。
20世紀40年代以前,人類一直未能掌握一種能高效治療細菌性感染且副作用小的藥物。當時若某人患了肺結核,那么就意味著此人不久就會離開人世。為了改變這種局面,科研人員進行了長期探索,然而在這方面所取得的突破性進展卻源自一個意外發現。
近代,1928年英國細菌學家弗萊明首先發現了世界上第一種抗生素—青黴素,亞歷山大·弗萊明由於一次幸運的過失而發現了青黴素。
1928年,英國科學家Fleming在實驗研究中最早發現了青黴素,但由於當時技術不夠先進,認識不夠深刻,Fleming並沒有把青黴素單獨分離出來。
1929年,弗萊明發表了他的研究成果,遺憾的是,這篇論文發表後一直沒有受到科學界的重視。
在用顯微鏡觀察這隻培養皿時弗萊明發現,黴菌周圍的葡萄球菌菌落已被溶解。這意味著黴菌的某種分泌物能抑制葡萄球菌。此後的鑑定表明,上述黴菌為點青黴菌,因此弗萊明將其分泌的抑菌物質稱為青黴素。然而遺憾的是弗萊明一直未能找到提取高純度青黴素的方法,於是他將點青黴菌菌株一代代地培養,並於1939年將菌種提供給準備系統研究青黴素的英國病理學家弗洛里(Howard Walter Florey)和生物化學家錢恩。
1938年,德國化學家恩斯特錢恩在舊書堆里看到了弗萊明的那篇論文,於是開始做提純實驗。
弗洛里和錢恩在1940年用青黴素重新做了實驗。他們給8隻小鼠注射了致死劑量的鏈球菌,然後給其中的4隻用青黴素治療。幾個小時內,只有那4隻用青黴素治療過的小鼠還健康活著。此後一系列臨床實驗證實了青黴素對鏈球菌、白喉桿菌等多種細菌感染的療效。青黴素之所以能既殺死病菌,又不損害人體細胞,原因在於青黴素所含的青黴烷能使病菌細胞壁的合成發生障礙,導致病菌溶解死亡,而人和動物的細胞則沒有細胞壁。
1940年冬,錢恩提煉出了一點點青黴素,這雖然是一個重大突破,但離臨床套用還差得很遠。
1941年,青黴素提純的接力棒傳到了澳大利亞病理學家瓦爾特弗洛里的手中。在美國軍方的協助下,弗洛里在飛行員外出執行任務時從各國機場帶回來的泥土中分離出菌種,使青黴素的產量從每立方厘米2單位提高到了40單位。
1941年前後英國牛津大學病理學家霍華德·弗洛里與生物化學家錢恩實現對青黴素的分離與純化,並發現其對傳染病的療效,但是青黴素會使個別人發生過敏反應,所以在套用前必須做皮試。所用的抗生素大多數是從微生物培養液中提取的,有些抗生素已能人工合成。由於不同種類的抗生素的化學成分不一,因此它們對微生物的作用機理也很不相同,有些抑制蛋白質的合成,有些抑制核酸的合成,有些則抑制細胞壁的合成。
通過一段時間的緊張實驗,弗洛里、錢恩終於用冷凍乾燥法提取了青黴素晶體。之後,弗洛里在一種甜瓜上發現了可供大量提取青黴素的黴菌,並用玉米粉調製出了相應的培養液。在這些研究成果的推動下,美國製藥企業於1942年開始對青黴素進行大批量生產。
到了1943年,製藥公司已經發現了批量生產青黴素的方法。當時英國和美國正在和納粹德國交戰。這種新的藥物對控制傷口感染非常有效。
1943年10月,弗洛里和美國軍方簽訂了首批青黴素生產契約。青黴素在二戰末期橫空出世,迅速扭轉了盟國的戰局。戰後,青黴素更得到了廣泛套用,拯救了數以千萬人的生命。到1944年,藥物的供應已經足夠治療第二次世界大戰期間所有參戰的盟軍士兵。因這項偉大發明,1945年,弗萊明、弗洛里和錢恩因“發現青黴素及其臨床效用”而共同榮獲了諾貝爾生理學或醫學獎。
1944年9月5日,中國第一批國產青黴素誕生,揭開了中國生產抗生素的歷史。截至2001年年底,中國的青黴素年產量已占世界青黴素年總產量的60%,居世界首位。
2002年,Birol等人提出了基於過程機理的模型,該過程綜合考慮了發酵中微生物的各種生理變化,發現這是個十分複雜的過程。為了更加方便地對青黴素過程進行研究,Birol對Bajpai和Reuss提出的非結構式模型進行了擴展,對模型進一步簡化,方便研究 。
主要功能
 二戰宣傳畫:感謝青黴素,傷兵可以安然回家
二戰宣傳畫:感謝青黴素,傷兵可以安然回家 青黴素是一種高效、低毒、臨床套用廣泛的重要抗生素。
它的研製成功大大增強了人類抵抗細菌性感染的能力,帶動了抗生素家族的誕生。它的出現開創了用抗生素治療疾病的新紀元。通過數十年的完善,青黴素針劑和口服青黴素已能分別治療肺炎、肺結核、腦膜炎、心內膜炎、白喉、炭疽等病。繼青黴素之後,鏈黴素、氯黴素、土黴素、四環素等抗生素不斷產生,增強了人類治療傳染性疾病的能力。但與此同時,部分病菌的抗藥性也在逐漸增強。為了解決這一問題,科研人員目前正在開發藥效更強的抗生素,探索如何阻止病菌獲得抵抗基因,並以植物為原料開發抗菌類藥物。
青黴素它不能耐受耐藥菌株(如耐藥金葡)所產生的酶,易被其破壞,且其抗菌譜較窄,主要對革蘭氏陽性菌有效。青黴素G有鉀鹽、鈉鹽之分,鉀鹽不僅不能直接靜注,靜脈滴注時,也要仔細計算鉀離子量,以免注入人體形成高血鉀而抑制心臟功能,造成死亡。
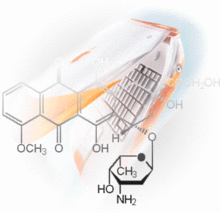 青黴素
青黴素 青黴素類抗生素的毒性很小,由於β-內醯胺類作用於細菌的細胞壁,而人類只有細胞膜無細胞壁,故對人類的毒性較小,除能引起嚴重的過敏反應外,在一般用量下,其毒性不甚明顯。
使用該品必須先做皮內試驗。青黴素過敏試驗包括皮膚試驗方法(簡稱青黴素皮試)及體外試驗方法,其中以皮內注射較準確。皮試本身也有一定的危險性,約有25%的過敏性休剋死亡的病人死於皮試。所以皮試或注射給藥時都應作好充分的搶救準備。在換用不同批號青黴素時,也需重作皮試。乾粉劑可保存多年不失效,但注射液、皮試液均不穩定,以新鮮配製為佳。而且對於自腎排泄,腎功能不良者,劑量應適當調整。此外,局部套用致敏機會多,且細菌易產生抗藥性,故不提倡。
組成分類
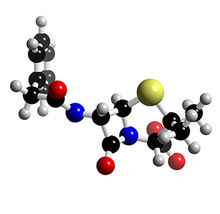 青黴素分子結構球棍模型
青黴素分子結構球棍模型 青黴素用於臨床是40年代初,人們對青黴素進行大量研究後又發現一些青黴素,當人們又對青黴素進行化學改造,得到了一些有效的半合成青黴素,70年代又從微生物代謝物中發現了一些母核與青黴素相似也含有β-內醯胺環,而不具有四氫噻唑環結構的青黴素類,可分為三代:第一代青黴素指天然青黴素,如青黴素G(苄青黴素);第二代青黴素是指以青黴素母核-6-氨基青黴烷酸(6-APA),改變側鏈而得到半合成青黴素,如甲氧苯青黴素、羧苄青黴素、氨苄青黴素;第三代青黴素是母核結構帶有與青黴素相同的β-內醯胺環,但不具有四氫噻唑環,如硫黴素、奴卡黴素。
按其特點可分為:
青黴素G類:如青黴素G鉀、青黴素G鈉、長效西林`青黴素G、peillin G、 盤尼西林、配尼西林、青黴素鈉、苄青黴素鈉、青黴素鉀、苄青黴素鉀等。
青黴素V類:(別名:苯氧甲基青黴素、6-苯氧乙醯胺基青黴烷酸)如青黴素V鉀等(包括有多種劑型)。
耐酶青黴素:如苯唑青黴素(新青Ⅱ號)、氯唑青黴素等。
抗假單胞菌青黴素:如羧苄西林、哌拉西林、替卡西林等。
美西林及其酯匹西林:如美西林及其酯匹美西林等,其特點為較耐酶,對某些陰性桿菌(如大腸、克雷伯氏和沙門氏菌)有效,但對綠膿桿菌效差。
甲氧西林類:如坦莫西林等。
藥理藥效
 青黴素——發現者
青黴素——發現者 青黴素類抗生素是β-內醯胺類中一大類抗生素的總稱,由於β-內醯胺類作用於細菌的細胞壁,而人類只有細胞膜無細胞壁,青黴素類抗生素的毒性很小,是化療指數最大的抗生素。但其青黴素類抗生素常見的過敏反應在各種藥物中居首位,發生率最高可達5%~10% ,為皮膚反應 ,表現皮疹、血管性水腫,最嚴重者為過敏性休克,多在注射後數分鐘內發生,症狀為呼吸困難、發紺、血壓下降、昏迷、肢體強直,最後驚厥,搶救不及時可造成死亡。各種給藥途徑或套用各種製劑都能引起過敏性休克,但以注射用藥的發生率最高。過敏反應的發生與藥物劑量大小無關。對該品高度過敏者,雖極微量亦能引起休克。注入體內可致癲癇樣發作。大劑量長時間注射對中樞神經系統有毒性(如引起抽搐、昏迷等),停藥或降低劑量可以恢復。
內服易被胃酸和消化酶破壞。肌注或皮下注射後吸收較快,15~30min達血藥峰濃度。青黴素在體內半衰期較短,主要以原形從尿中排出。
青黴素藥理作用是干擾細菌細胞壁的合成。青黴素的結構與細胞壁的成分粘肽結構中的D-丙氨醯-D-丙氨酸近似,可與後者競爭轉肽酶,阻礙粘肽的形成,造成細胞壁的缺損,使細菌失去細胞壁的滲透屏障,對細菌起到殺滅作用。
聯合反應
臨床中出現濫用藥物的問題,造成一些不良反應,尤其是青黴素與其他藥物的配伍套用,所產生的相互作用和不良反應是不可忽視的。
1、青黴素不可與同類抗生素聯用
由於它們的抗菌譜和抗菌機制大部分相似,聯用效果並不相加。相反,合併用藥加重腎損害,還可以引起呼吸困難或呼吸停止。它們之間有交叉抗藥性,不主張兩種β-內醯胺類抗生素聯合套用。
2、青黴素不可與磺胺類藥物和四環素類藥物聯合使用
青黴素屬繁殖期“殺菌劑”,阻礙細菌細胞壁的合成,四環素屬“抑菌劑”,影響菌體蛋白質的合成,二者聯合作用屬拮抗作用,一般情況下不應聯合用藥。臨床資料表明單用青黴素抗菌效力為90%,單用磺胺類藥效力為81%,兩者聯合用藥抗菌效力為75%,若非特殊情況不可聯合使用。
3、青黴素不可與氨基糖苷類混合輸液
兩者混契約於輸液器給病人輸液,因青黴素的β-內醯胺可使慶大黴素產生滅活作用,其機制為兩者之間發生化學相互作用,故嚴禁混合套用,應採用青黴素靜脈滴注,慶大黴素肌肉注射。
綜上所述,青黴素聯用不當,由於藥物的相互作用,而導致藥物不良反應是不可低估的。青黴素是治療各種感染性疾病的最常用抗生素,嚴格掌握用藥的適應證,合理聯用,措施得力,減少不必要的不良反應。
4、氯黴素、紅黴素、四環素類、磺胺藥等抑菌劑可干擾青黴素的殺菌活性,不宜與青黴素類合用,尤其是在治療腦膜炎或需迅速殺菌的嚴重感染時。
5、丙磺舒、阿司匹林、吲哚美辛、保泰松、磺胺藥可減少青黴素類在腎小管的排泄,因而使青黴素類的血藥濃度增高,而且維持較久,半衰期延長,毒性也可能增加。
6、青黴素鉀或鈉與重金屬,特別是銅、鋅和汞呈配伍禁忌,因後者可破壞青黴素的氧化噻唑環。由鋅化合物製造的橡皮管或瓶塞也可影響青黴素活力。呈酸性的葡萄糖注射液或四環素注射液皆可破壞青黴素的活性。青黴素也可為氧化劑或還原劑或羥基化合物滅活。
7、青黴素靜脈輸液加入頭孢噻吩、林可黴素、四環素、萬古黴素、琥乙紅黴素、兩性黴素B、去甲腎上腺素、間羥胺、苯妥英鈉、鹽酸羥嗪、丙氯拉嗪、異丙嗪、維生素B族、維生素C等後將出現混濁。故該品不宜與其他藥物同並滴注。
8、青黴素可增強華法林的作用。
9、該品與氨基糖苷類抗生素混合後,兩者的抗菌活性明顯減弱,因此兩藥不能置同一容器內給藥。
藥物毒性
青黴素過敏
口服後吸收迅速,約75%-90%可自胃腸道吸收,食物對藥物吸收的影響不顯著,它的蛋白結合率為17%-20%,血消除半衰退期(t1/2)為1到1.3小時,服藥後約24%-33%的給藥量在肝內代謝,6小時內46%-68%給藥量以原型藥自尿排出,尚有部分藥物經過膽道排泄,嚴重腎功能不全患者血清半衰期可延長至7小時。血清透析可清除青黴素,腹膜透析則無清除該品的作用。
青黴素是各類抗生素中毒副作用最小的,因為其作用機理在於破壞細胞壁形成過程和結構,而人體沒有細胞壁。青黴素對人體基本沒有藥理毒性,但大劑量青黴素也可能導致神經系統中毒。青黴素的副作用主要原因在於青黴素的提純不足,其中的雜質容易使人體過敏。
⒈過敏反應:青黴素過敏反應較常見,在各種藥物中居首位。嚴重的過敏反應為過敏性休克(Ⅰ型變態反應)發生率為0.004%~0.015%,Ⅱ型變態反應為溶血性貧血、藥疹、接觸性皮炎、間質性腎炎、哮喘發作等,Ⅲ型變態反應即血清病型反應亦較常見,發生率為1%~7%。過敏性休克不及時搶救者,病死率高。因此,一旦發生必須就地搶救,立即給病人肌注0.1%腎上腺素0.5~1ml,必要時以5%葡萄糖或氯化鈉注射液稀釋作靜脈注射,臨床表現無改善者,半小時後重複一次。心跳停止者,腎上腺素可作心內注射。同時靜脈滴注大劑量腎上腺皮質激素,並補充血容量;血壓持久不升者給予多巴胺等血管活性藥。亦可考慮採用抗組胺藥以減輕蕁麻疹。有呼吸困難者予氧氣吸入或人工呼吸,喉頭水腫明顯者應及時作氣管切開。青黴素酶套用意義不大。
⒉毒性反應:青黴素毒性反應較少見,肌注區可發生周圍神經炎。鞘內注射超過2萬單位或靜脈滴注大劑量青黴素可引起肌肉陣攣、抽搐、昏迷等反應(青黴素腦病),多見於嬰兒、老年人和腎功能減退的病人。青黴素偶可致精神病發作,套用普魯卡因青黴素後個別病人可出現焦慮、發熱、呼吸急促、高血壓、心率快、幻覺、抽搐、昏迷等。此反應發生機制不明。
⒊二重感染:用青黴素治療期間可出現耐青黴素金葡菌、革蘭陰性桿菌或白念珠菌感染,念珠菌過度繁殖可使舌苔呈棕色甚至黑色。
⒋高鉀血症(低鉀血症)與高鈉血症:如靜脈給予大量青黴素鉀時,可發生高鉀血症或鉀中毒反應。大劑量給予青黴素鈉,尤其是對腎功能減退或心功能不全病人,可造成高鈉血症。每日給予病人1億單位青黴素鈉後,少數病人可出現低鉀血症、代謝性鹼中毒和高鈉血症。
⒌赫氏反應和治療矛盾:用青黴素治療梅毒、鉤端螺鏇體病或其他感染時可有症狀加劇現象,稱赫氏反應,系大量病原體被殺滅引起的全身反應。治療矛盾也見於梅毒病人,系由於治療後梅毒病灶消失過快,但組織修補較慢,或纖維組織收縮,妨礙器官功能所致。
6.獸醫臨床上的過敏一般較輕,主要表現為流汗、興奮、不安、肌肉震顫、呼吸困難、心率加快、站立不穩、有時見蕁麻疹、眼瞼和面部水腫,陰門和直腸腫脹和無菌性蜂窩織炎、嚴重時休克甚至死亡。
原因
青黴素不穩定,可以分解為青黴噻唑酸和青黴烯酸。前者可聚合成青黴噻唑酸聚合物,與多肽或蛋白質結合成青黴噻唑酸蛋白,為一種速發的過敏源,是產生過敏反應最主要的原因;後者還可與體內半胱氨酸形成遲發性致敏原-青黴烯酸蛋白,與血清病樣反應有關。有藥物過敏史或者變態反應性患者,在局部用藥及長效製劑的時候發生率較高。
臨床使用中,應該避免高溫、酸鹼、以及重金屬離子的侵襲。儘量避免使用PH值顯酸性的葡萄糖注射液做溶媒,而在使用0.9%的氯化鈉做溶媒時,也應該做到現用現配,否則放置時間過長,也會引起青黴素的分解,而致過敏反應的發生。
急救措施
⒈立即停藥,平臥,就地搶救,採用頭低足高位。
⒉皮下注射 0.1% 鹽酸腎上腺素 0.5-1 毫升,兒童酌減,每隔半小時可再皮下注射 0.5 毫升,直至脫離危險期,必要時加糖皮質激素或抗組胺藥。
⒊心臟停跳者,行心臟胸外按壓術或心內注射 0.1% 鹽酸腎上腺素 1 毫升。
⒋吸氧,呼吸抑制時口對口人工呼吸,並肌肉注射尼可剎米或山梗菜鹼等呼吸中樞興奮劑。
喉頭水腫影響呼吸時行氣管切開術。
⒌用氫化考的松 200 毫克,或地塞米松5-10 毫克加入 50%Glucose40 毫升中靜脈注射,或加入 5-10%Glucose500 毫升中靜滴。
⒍根據病情需要可用血管活性藥物如多巴胺,阿拉明等。
⒎糾正酸中毒及組織胺藥物的套用。
⒏注意保暖,防止感冒,要做好護理記錄,不要搬動。
⒐可針刺人中,內關,印堂,合谷,湧泉等急救穴位。
⒑可用艾條灸內關,合谷,湧泉,關元,中脘等穴位。
青黴素腦病
青黴素腦病是青黴素的一種少見中樞神經系統毒性反應,通常青黴素僅有少量通過血腦屏障,但在用量過大,靜滴速度過快時,大量藥物迅速進入腦組織,即血及腦脊液中藥物的濃度升高,干擾正常的神經功能致嚴重的中樞神經系統發應,如反射亢進、知覺障礙、幻覺、抽搐、昏睡等,稱之“青黴素腦病”。
青黴素腦病的發病機理未明,其原因是藥物在一定程度上抑制了中樞神經抑制性遞質γ-氨基丁酸(GABA)的合成和轉運,並抑制中樞神經細胞Na+-K+-ATP酶,使靜息膜電位降低所致。有文獻認為可能與青黴素鈉鹽中的陽離子有關,認為鈉、鋰、銨、鍶、鈣、鎂、鉀的毒性作用依次增大,此外與製劑純度,個體差異,劑量大小、注射方 法,速度、濃度均有關。有的學者證明青黴素G在腦脊液中的濃度超過8u~10u/ml,即可出現毒性反應,有人認為血腦屏障機能差是主要原因。青黴素進入機體後90%由腎臟排出,嬰兒腎功能差,使其半衰期延長,血中濃度增高,毒性增加,發生神經毒性作用。導致大腦興奮性增高——驚厥,即“青黴素腦病。目前主張嬰兒青黴素用量7天每8小時1次,嚴重感染每6小時1次。
⒋早產兒劑量:第1周3萬U/kg,每l2小時1次,2~4周時每8小時l次,以後每6小時1次。
製劑與規格
1、注射用青黴素鈉:①0.12g(20萬U);②0.24g(40萬U);③0.48g(80萬U);④0.6g(100萬U);⑤0.96g(160萬U;⑥2.4g(400萬U)。
2、 注射用青黴素鉀:①0.125g(20萬U);②0.25g(40萬U);③0.5g(80萬U);④0.625g(100萬U)。
細菌耐藥性
金黃色葡萄球菌對青黴素最易產生耐藥性。細菌對青黴素類產生耐藥性主要有三種機制:
⒈細菌產生β內醯胺酶,使青黴素類水解滅活
⒉細菌體內青黴素作用靶位——青黴素結合蛋白發生改變
⒊細胞壁對青黴素類的滲透性減低。
其中以第一種機制最為常見,也最重要。
青黴素類抗生素水溶性好,血消除半衰期大多不超過2小時,主要經腎排出,多數品種可經血液透析清除。
按中國衛生部規定,使用青黴素類抗生素前均需做青黴素皮膚試驗,陽性反應者禁用。
研究進展
青黴素(盤尼西林)是抗生素界的鼻祖,作為20世紀的一項科學奇蹟,它的抗菌能力已經大大降低。美國南卡羅來納大學的科學家Chuanbing Tang和他的同事們發現了一種新方法能夠恢復青黴的抗菌活性,甚至可以對抗“超級細菌”,相關研究發表在近期《美國化學學會》期刊上。
20世紀40年代,因抗生素被大規模使用,使得細菌對青黴素家族藥物產生了耐藥性。比如,金黃色葡萄球菌引起的葡萄球菌感染可使用青黴素及其結構類似物進行治療。但細菌是在不斷變化的,經過一系列進化,金黃色葡萄球菌變成耐甲氧西林金黃色葡萄球菌(MRSA)。老一代抗生素對MRSA不起作用,一個重要原因是MRSA能夠將其強大的抗菌活性無效化。
原來,青黴素的抗菌活性來自它的分子結構核心:含有氨基的四元環——“β-內醯胺”。它是青黴素及其衍生物均具有的結構單元,人們把具有這個結構單元的藥物家族稱為“β-內醯胺類抗生素”。β-內醯胺能夠十分有效地阻止細菌的細胞分裂,因此化學家們一直在合成含有β-內醯胺結構的不同修飾基團的藥物,但很多藥物已經不再具有抗菌活性而被淘汰。
細菌耐藥的一個重要機制就是它們含有一種“β-內醯胺酶”,能夠水解β-內醯胺結構。比如MRSA能夠通過生物途徑合成並釋放β-內醯胺酶,而且這種酶的作用範圍十分廣泛。
注意事項
⒈口服或注射給藥時忌與鹼性藥物配伍,以免分解失效。
⒉該品不宜與鹽酸四環素、卡那黴素、多粘菌素E、磺胺嘧啶鈉、三磷酸腺苷、輔酶A等混合靜滴,以免發生沉澱或降效。
⒊氯黴素與青黴素一般不要聯用,因氯黴素為抑菌劑,而青黴素為繁殖期殺菌劑,聯用可影響青黴素的抗菌活性而降效。但這一問題尚有爭論,意見不一,因兩者聯用對革蘭陽性菌、陰性菌混合感染及顱內感染臨床效果好。解決的辦法,如需聯用,宜先用青黴素2~3小時後再用氯黴素。
⒋由於該品可抑制某些肝臟酶的活性,因此可干擾甲苯磺丁脲、苯妥英鈉和雙香豆素在人體內的生物轉化,可增強甲苯磺西脲、苯妥英鈉的作用,對雙香豆素和華法林的抗凝作用均可增強。
⒌嬰兒、肝、腎功能減退者慎用,妊娠末期產婦慎用,哺乳期婦女忌用。
套用青黴素前除做皮試外,還要注意以下幾點:
⒈要到有搶救設備的正規醫療單位注射青黴素,萬一發生過敏反應,可以得到及時有效的搶救治療。在注射過程中任何時候出現頭暈心慌、出汗、呼吸困難等不適,都要立即告訴醫生護士。
⒉注射完青黴素,至少在醫院觀察20分鐘,無不適感才可離開。
⒊不要在極度飢餓時套用青黴素,以防空腹時機體對藥物耐受性降低,誘發暈針等不良反應。
⒋兩次注射時間不要相隔太近,以4—6小時為好。靜脈點滴青黴素時,開始速度不要太快,每分鐘以不超過40滴為宜,觀察10—20分鐘無不良反應再調整輸液速度。
⒌如果當天有注射青黴素史,在家中出現頭暈心慌、出汗、呼吸困難等不適,應及時送醫院診治。
氨苄青黴素注意七點:
氨苄青黴素(包括含氨苄青黴素的安滅菌等)是青黴素類藥中分解最快、過敏反應發生率最高的一種,尤其在酸性環境中和血藥濃度高的情況下,更易發生氨苄青黴素分解產物、疊合物堆積所致的過敏性藥疹、過敏性休克,甚至因此而危及生命。在臨床使用氨苄青黴素時,不僅要做皮試,還應注意以下幾點:
一是皮試陰性,並不意味著不過敏。氨苄青黴素過敏反應多為遲發性,可在連續用藥數天后才出現過敏性藥疹,致過敏性休克。對過敏性藥疹,在停藥後使用息斯敏、苯海拉明、地塞米松可以解決。對突然發生呼吸困難、寒戰發熱、血壓下降、心率加快等症狀者,要立即停藥,並給氧,使用腎上腺素、地塞米松、葡萄糖酸鈣等藥搶救。
二是宜短期使用,切忌長期大量給藥,以免血藥濃度持續升高,導致致敏物質的形成與堆積,造成過敏反應。
三是宜在足量生理鹽水中充分溶解後靜脈滴注。一般而言,4克的氨苄青黴素需在300毫升左右的生理鹽水(0.9%氯化鈉注射液)中溶解。絕對不能溶解在糖,特別是高滲糖(濃度大於5%的葡萄糖注射液)中靜脈滴注。因糖呈酸性,不僅可降低氨苄青黴素的抑菌、殺菌能力,而且可促使自身分解,增加致敏機會。
四是痛風、尿毒症、糖尿病酮症酸中毒和乳酸酸中毒患者應儘量少用或不用氨苄青黴素。原因也是氨苄青黴素在酸性環境中可促使自身分解而增加致敏可能。
五是患者本身為過敏體質者,應避免使用。
六是通常靜脈給藥,宜慢不宜快,以每分鐘不超過60滴的速度靜脈滴注,以免血藥濃度增高過快而增加分解過敏可能。
七是在使用之前,應找到對本藥敏感的致病菌感染的確切證據,切忌盲目濫用,以免因此造成菌群失調、黴菌感染而增加治療難度。
禁忌證:對任何青黴素類過敏的患者禁用該品。
過敏原理
青黴素不穩定,可以分解為青黴噻唑酸和青黴烯酸。前者可聚合成青黴噻唑酸聚合物,與多肽或蛋白質結合成青黴噻唑酸蛋白,為一種速發的過敏源,是產生過敏反應最主要的原因;後者還可與體內半胱氨酸形成遲發性致敏原-青黴烯酸蛋白,與血清病樣反應有關 。
藥物標準
與青黴素有關的國家基本藥物零售指導價格信息
| 序號 | 基 本藥 物 目錄序號 | 藥品名稱 | 劑型 | 規格 | 單位 | 零售指 導價格 | 類別 | 備註 |
| 1 | 1 | 青黴素 | 注射劑 | 80萬單位 | 瓶(支) | 1元 | 化學藥品和 生物製品 部分 | * |
| 2 | 1 | 青黴素 | 注射劑 | 160萬單位 | 瓶(支) | 1.8元 | 化學藥品和生物製品部分 | |
| 3 | 1 | 青黴素 | 注射劑 | 400萬單位 | 瓶(支) | 3.5元 | 化學藥品和生物製品部分 | |
| 4 | 1 | 青黴素 | 注射劑 | 800萬單位 | 瓶(支) | 5.5元 | 化學藥品和生物製品部分 |
說明:
⒈表中備註欄標註“*”的為代表品。
⒉表中代表劑型規格在備註欄中加注“△”的,該代表劑型規格及與其有明確差比價關係的相關規格的價格為臨時價格。
⒌腎功能減退病人劑量:腎小球濾過率(GFR)為10~15ml/min時,給藥間歇自8小時延長至8~12小時或劑量減少25%。當GFR少於10ml/min時,給藥間歇為12~18小時或劑量減至正常劑量的25%~50%。一般說來病人腎功能損害屬輕中度者,使用常規劑量,不需減量,腎功能損害嚴重者再調整劑量或延長給藥時間。