固體發光
正文
電磁波、帶電粒子、電能、機械能及化學能等作用到固體上而被轉化為光能的現象。它有兩個基本特徵:第一,任何物體在一定溫度下都有熱輻射,發光是物體吸收外來能量後所發出的總的輻射中超出熱輻射部分;第二,當外界激發源對固體的作用停止後,發光還延續一段時間,稱為餘輝。不同材料在不同激發方式下的發光過程可以很不相同,但有一個共同點:都是固體從高激發態到低激發態(特別是基態)的電子躍遷中釋放能量的一個方式。固體發光的激發方式是其技術套用的依據,主要有以下幾類。
① 射線的激發。可分為:(a)電磁波激發包括光頻、X 射線及γ射線等各個波段的電磁波都可激發發光體。近代同步輻射的利用,把光頻激發源擴展到短波紫外直至和X射線波段銜接起來。(b)粒子激發主要是帶電粒子,如電子、質子及離子等轟擊發光體形成的激發。
② 電激發。在發光體內直接將電能轉換為光能。電致發光一般要求發光體有足夠的導電性。
③ 化學發光。化學反應中釋放出來的能量也可在一定條件下激發材料,使材料發光。
④ 摩擦發光及結晶發光。這是在機械壓力下晶體破裂所引起的閃光及晶體從溶液或熔體中生長時的發光。
⑤ 生物發光。在生物體內由於生命過程中的變化所產生的發光。
發光學從它的光譜研究(斯托克斯定則,1852)及動力學研究(貝可勒爾公式,1867)開始,至G.H.維德曼(1888)才提出“發光”這個概念。但他只注意到發光同熱輻射的區別。1936年С.И.瓦維洛夫把發光期間(即餘輝)作為發光現象的另一個主要判據以後,發光才有了確切的科學定義。固體中的發光過程大致分為兩大類:分立中心的發光,發光的全部過程都局限在單箇中心的內部(單分子過程);複合發光,發光過程中經過電離(電子脫離母體或發光中心),電子同電離中心複合而發光(雙分子過程)。
1950年以後,由於理論方法、實驗技術、材料提純及製備等方面的進展,工業產生對發光的與日俱增的需要,以及若干邊緣學科,包括雷射、光電子學、光化學反應、光合作用及發光分析等對發光現象的興趣,促使發光學的研究進入了一個新的階段。它的主要特徵是把發光現象溯源於固體的基本性質,包括光和物質的相互作用,固體的結構、雜質和缺陷,電子能譜的結構,半導體的物理過程,點陣振動,表面及界面以及環境條件的影響等。從而使發光理論建基於固體物理,特別是固體的光學性質及其電子過程上。發光體的種類很多,從結構上看,它們的發光幾乎都和固體中的缺陷和雜質有關。從實用出發,對發光的研究一直側重在可見光範圍。為了避免發光的再吸收,所用的主體材料(稱為基質)是寬禁帶的半導體、半絕緣體及絕緣體。在這些材料中,很多情況是分立中心發光,它的主要特徵取決於中心性質及其環境;而複合發光則和載流子在材料中的運動有關。
分立中心的發光 這是在絕緣體發光中的主要類型。常用的基質材料包括:鹼金屬鹵化物,如NaCl;鹼土金屬鹵化物,如CaF2;氧化物,如Al2O3、MgO、Y3Al5O12;鎢酸鹽、矽酸鹽、鉬酸鹽、鍺酸鹽等,如CaWO4;玻璃等。在某些Ⅱ-Ⅵ族化合物,如ZnS;Ⅲ-Ⅴ族化合物,如GaN;以及金剛石等寬禁帶半導體材料中有些雜質也可形成分立發光中心。常用的形成分立中心的雜質有:①過渡金屬離子,其外殼層是3d電子,如Cr3+(3d3)、Mn2(3d3)②稀土元素的離子,其三價離子的外殼層都是4f電子,二價Ce、Gd、Tb等是5d電子。③錒系元素的離子。④類汞離子,這是Hgo的等電子離子,外殼層是ns2電子,如Zno、Cao、Hgo、Ca+、In+、Tl+、Ge2+、Sn2+、Pb2+、Bi3+等。當這些摻雜離子在基質中的濃度很低時,彼此幾乎沒有影響。發光來自孤立的雜質離子。
這些雜質離子在自由狀態時可以具有一定的能譜,並且按照自鏇、宇稱等選擇定則,發生能級之間的光學躍遷。如果把這類雜質摻到固體中,它周圍的基質離子就會通過和雜質離子之間的庫侖作用而對後者發生影響。雜質離子所感受的庫侖場的總和稱為它所在位置上的晶體場。在計算雜質離子的波函式及其能量本徵值時,就必須考慮到這些周圍離子的影響。
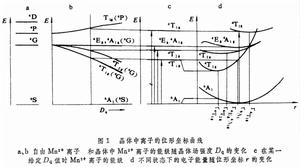
以Mn2+為例,它在自由離子狀態時的能級如圖1a。把它摻進氧化物中時,它取代了正離子,近鄰有二個氧離子,Mn2+到它們平衡位置的距離相等,形成一個八面體。由於這一環境的晶體場的作用,使Mn2+的能級發生了劈裂。A1、T1、T2、E等是用群論符號對離子在八面體晶體場中的電子軌道對稱性的標記。下標g表示偶宇稱,u表示奇宇稱。隨著晶體場強度Dq的改變,劈裂能級有不同的變化。這是由於它們來源於不同的電子軌道(圖1b)。
 固體發光
固體發光由於電子質量遠小於原子核,當雜質離子的電子從基態躍遷到激發態時,原子核的位置還來不及改變,發生豎直躍遷。在電子處於激發態的期間,環境離子通過點陣振動的弛豫,移到新的平衡位置;電子能量下降到激發態的能量極小值附近。又通過豎直躍遷回到基態。這種豎直躍遷被稱為夫蘭克-康登原理。從圖1d可以看出,這時發射光譜相對吸收光譜移向長波,稱為斯托克斯位移。斯托克斯位移相應於伴隨電子躍遷產生很多聲子。根據以上分析,吸收光譜及發射光譜的譜帶都將變寬。稀土離子和點陣的相互作用弱,發光的譜帶窄,這一位移很小,無法測出;Mn2+和點陣相互作用較強,它的發光帶變寬,位移也大;F心的譜帶更寬,這一位移可大到1eV。
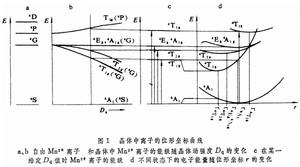
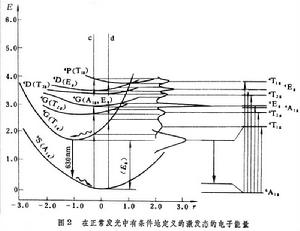
位形坐標曲線是一種統一地考慮雜質和環境的相互作用,並做出一些簡化近似所得到的結果。先前用它定性地解釋一些現象,近期才開始分析數量關係。過去只觀察到正常的發光,它都是從激發態的極小位置發生電子躍遷的,所以有條件地(即僅就正常發光而論)定義激發態的極小值及基態的極小值之間的能量差<Ee>為電子能量,而把躍遷達到的能級多於<Ee>的部分歸之為振動能。現在關於過熱發光的實驗證明,處於激發態的電子可以從高過<Ee>的電子態發生躍遷(圖2)。從圖2 還可看到,儘管Mn2+可以有幾個吸收帶,但發光卻只有一個譜帶。這說明被激發到較高激發態的電子都必須先弛豫到最低激發態,然後才躍遷到基態。而在相鄰的兩個激發態之間的躍遷是無輻射躍遷。能級間的能量差越大,無輻射躍遷的幾率越小。無輻射躍遷的幾率 p和能級間的距離ΔE及聲子能量媡ω的關係可表示為
 。
。
 固體發光
固體發光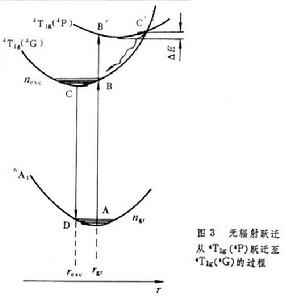 固體發光
固體發光在固體中由於存在大量缺陷及其他雜質,常能形成複雜的發光中心,如F心是鹼金屬鹵化物中陰離子空位上俘獲了一個電子所形成的。也可以分子形式摻雜,形成分子中心。這類研究要利用分子軌道理論。
實用上常選用絕緣體或半絕緣體(作為基質)及合適的中心,形成分立中心的發光。
複合發光 這類發光多見於半導體,它受到激發後,摻雜離子或基質離子都可能被電離。例如,在ZnS中禁頻寬度是3.83eV,以波長短於325nm的光照射它,會發生電子從價帶至導帶的躍遷:
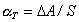 。
。
複合發光取決於能帶結構。摻雜半導體中發光又與雜質引進的能級位置有關。從對電學性質的影響上區分,有三類雜質:施主、受主和等電子雜質。當發光體被激發後,施主可以俘獲一個電子,受主可以俘獲一個空穴,等電子雜質可以明顯地提高發光效率。
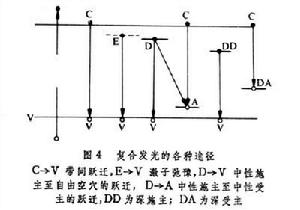
複合發光的主要特點是導帶電子和價帶空穴參與發光。有各種複合過程(圖4)。這些電子躍遷中,既要求能量守恆,又要求動量守恆。在直接帶隙材料內,導帶極小及價帶極大都位於波矢值k為0處,帶間的躍遷是豎直的。而在間接帶材料中,導帶極小及價帶極大不在同一k值處,帶間躍遷需要有聲子參與,所以躍遷幾率比前者小(圖5)。
 固體發光
固體發光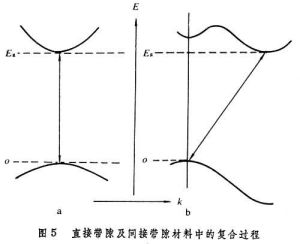 固體發光
固體發光利用順磁共振譜(見磁共振)隨著雜質中心的電離而發生的變化,可以了解雜質中心的來源及性質。通過雜質中心的複合發光有三類:施主俘獲的電子同價帶內空穴的複合,受主俘獲的空穴和導帶內電子的複合及施主的電子同受主的空穴的複合(圖4)。
半導體的發光常包括複合發光和分立中心的發光。例如,當Mn2+或三價稀土離子在ZnS中形成雜質中心時,表現出分立中心的特徵。半導體發光的另一個重要特點是可在外電場直接作用下發光,稱為電致發光。
電子激發態的運動──能量傳遞 除去上述分立中心的激發及半導體中基質或雜質中心的電離等激發態外,常見的電子激發態還有激子。這是導帶中的電子及價帶中的空穴在庫侖引力下結合在一起的一種狀態。它的能量略低于禁頻寬度。這三類激發都可在固體中運動。這些運動在很大程度上影響發光的光譜及發光的效率。
分立中心之間的能量傳遞,常見的有兩種表現:①摻入兩種雜質時,對應於一種雜質的發光減弱了(直至消失)而對應於另一種雜質的發光得到增強。②一種雜質的發光並非來源於它的激發光譜範圍內的光激發,而來源於另一種雜質的激發或吸收光譜範圍內的光激發。前者稱激活中心,後者稱敏化中心。能量傳遞在發光弛豫速率方面的表現是敏化中心的發光餘輝變短,因為這時增多了一條能量弛豫的途徑。能量傳遞的主要方式有以下幾種:
尋常的再吸收 ① 共振無輻射傳遞。它來源於兩個中心之間的庫侖作用,要求敏化中心及激活中心的電子躍遷有相當的能量差。但並不要求敏化中心的躍遷伴有發光,也不要求與這一躍遷相對應的激活中心的吸收很強。只要敏化中心的吸收強,激活中心的發光好,就可獲得有效的能量傳遞。傳遞幾率與中心的性質和中心之間的相對距離有關。如果是偶極子到偶極子的傳遞,其幾率與離子間的作用距離r的六次方成反比;如果是偶極子與四極子的傳遞,則傳遞幾率與r的八次方成反比。前者的有效距離約達30┱,後者的則更短,約10~12┱。
② 非共振無輻射傳遞。當兩個中心的電子躍遷能量不相等時,需要藉助於聲子,以達到能量平衡。這是一種有聲子協助的過程,必須考慮敏化及激活中心與環境離子的相互作用。一般說,它的傳遞幾率不如共振傳遞的幾率大。
藉助於載流子的傳遞 在半導體中,載流子的漂移及其被雜質中心的俘獲,是將激發態從一個中心傳遞到另一中心的獨特的途徑。
藉助於激子的傳遞 激子可以在晶體中運動也可將激發能量帶走,傳遞給其他中心。
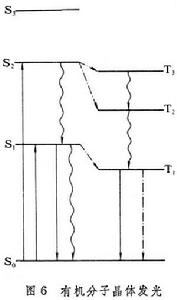
有機分子晶體的發光 在范德瓦耳斯力的作用下結合在一起的晶體中,其分子間的相互作用很弱。任何含有非局域π電子的分子都有一定的發光能力。π鍵包含兩個電子,自鏇相反,所以基態都是單態。激發態則有單態,也有三重態。按照量子力學的要求,二者之間的躍遷是禁戒的。單態的能級總是高於相應的三重態的能級。處於任一單態的電子都可產生髮光,但由於從高激發態到低激發態有內部轉換(無輻射躍遷),發光一般是從最低激發態到基態的躍遷。π 電子的發光躍遷示意如圖6,從S1到So的發光躍遷稱為螢光。從T1到So的發光躍遷稱為磷光。處於 T1態的分子在熱騷動下也可回到S1態,從S1又返回到So的發光稱為延遲發光。在單態及三重態之間仍然有一定的無輻射能量傳遞過程,稱為交叉弛豫。交叉弛豫的幾率都隨兩個能級之間能隙的增大而減少。
 固體發光
固體發光有機分子間的能量傳遞是很有效的。在晶體中分子的濃度極高,傳遞速度更快。單態之間的能量傳遞進行得很快,被稱為單態激子傳遞。三重態也是這樣,也可稱為三重態激子傳遞。三重態激子相互碰撞時也可發生向單態的躍遷
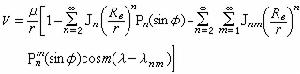 ,
,
發光的技術套用 主要有四個方面。
照明技術及特殊需要的光源 如日光燈、高壓汞燈、黑光燈、發光二極體等。在光通信技術中可調製的光源可以充當信息源,一般光源也可通過對其光束的調製充當信息載體。
顯示顯像技術 如數字元號顯示、矩陣及模擬顯示;又如電視屏、微光夜視、紅外變像、X射線轉換屏等。
雷射工作物質 包括利用發光材料產生雷射以及雷射光頻變換等。
探測技術 利用發光的主要特徵參量,如光譜、衰減、偏振等,探測輻照強度、生物組織、分析化學組成及分子物理過程等。
參考書目
M.D. Lumb, Luminescence Spectroscopy, AcademicPress, London, New York, San Francisco, 1978.
W. M. Yen and P. M.Selzer, Lαser Spectroscopy of Solids, Springer-Verlag, Berlin, Heidelberg, New York,1981.
中國科學院吉林物理研究所、中國科學技術大學,《固體發光》編寫組編:《固體發光》,中國科學技術大學出版,合肥,1976。